题目内容
已知下列热化学方程式:
(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
(3)H2(g)+
O2(g)═H2O(l)△H3=-285.8kJ/mol
则反应2C(s)+2H2(g)+O2(g)═CH3COOH(l)的焓变为( )
(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
(3)H2(g)+
| 1 |
| 2 |
则反应2C(s)+2H2(g)+O2(g)═CH3COOH(l)的焓变为( )
分析:依据热化学方程式和盖斯定律计算分析,反应的焓变与反应过程无关,只与起始状态和终了状态有关.
解答:解:(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
(3)H2(g)+
O2(g)═H2O(l)△H3=-285.8kJ/mol
依据盖斯定律(2)×2-(1)+(3)×2得到
2C(s)+2H2(g)+O2(g)═CH3COOH(l)△H=-488.3 kJ/mol,
故选:A.
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
(3)H2(g)+
| 1 |
| 2 |
依据盖斯定律(2)×2-(1)+(3)×2得到
2C(s)+2H2(g)+O2(g)═CH3COOH(l)△H=-488.3 kJ/mol,
故选:A.
点评:本题考查热化学方程式的书写和盖斯定律的计算应用,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
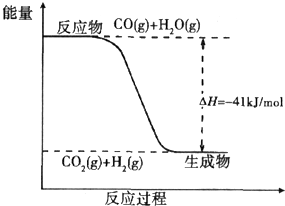 煤炭可以转化为清洁能源和化工原料.
煤炭可以转化为清洁能源和化工原料.