题目内容
下列水解反应的离子方程式正确的是( )
| A.NH4++H2O?NH3?H2O+H+ |
| B.S2-+H2O?H2S+2OH- |
| C.CH3COOH+H2O?CH3COO-+H+ |
| D.CH3COOH+OH-?CH3COO-+H2O |
A.铵根离子为弱碱离子,水解离子反应为NH4++H2O?NH3?H2O+H+,故A正确;
B.硫离子为多元弱酸根离子,水解以第一步为主,则水解离子反应为S2-+H2O?HS-+OH-,故B错误;
C.不遵循质量守恒定律,且醋酸为弱电解质,不能水解,其电离方程式为CH3COOH?CH3COO-+H+,故C错误;
D.醋酸为酸,与碱反应生成盐和水,则CH3COOH+OH-═CH3COO-+H2O为中和反应的离子反应,不需要使用“?”,故D错误;
故选A.
B.硫离子为多元弱酸根离子,水解以第一步为主,则水解离子反应为S2-+H2O?HS-+OH-,故B错误;
C.不遵循质量守恒定律,且醋酸为弱电解质,不能水解,其电离方程式为CH3COOH?CH3COO-+H+,故C错误;
D.醋酸为酸,与碱反应生成盐和水,则CH3COOH+OH-═CH3COO-+H2O为中和反应的离子反应,不需要使用“?”,故D错误;
故选A.

练习册系列答案
相关题目
 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
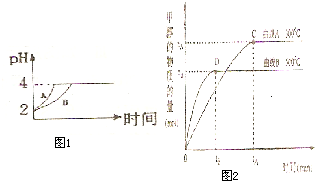
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: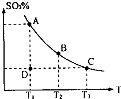 (1)在硫酸生产中,SO2催化氧化生成SO3是反应的关键,其反应的化学方程式为:2SO2(g)+O2(g)?2SO2(g),反应混合体系SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题:
(1)在硫酸生产中,SO2催化氧化生成SO3是反应的关键,其反应的化学方程式为:2SO2(g)+O2(g)?2SO2(g),反应混合体系SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题: 铜是人类最早使用的金属,被广泛应用于电气、轻工、机械制造和国防工业等.已知Cu2O与H2SO4能发生反应:Cu2O+H2SO4=Cu+CuSO4+H2O.
铜是人类最早使用的金属,被广泛应用于电气、轻工、机械制造和国防工业等.已知Cu2O与H2SO4能发生反应:Cu2O+H2SO4=Cu+CuSO4+H2O. 4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。
4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。