题目内容
将amolNa2O2和bmolNaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应.当剩余固体为Na2CO3、NaOH,排出气体为O2、H2O时,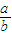 值可能为( )
值可能为( )A.0.5
B.0.65
C.0.85
D.1.0
【答案】分析:混合物在密闭容器中加热到250℃时,可能发生如下反应:??①2NaHCO3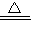 Na2CO3+CO2↑+H2O↑
Na2CO3+CO2↑+H2O↑
②2Na2O2+2CO2=2Na2CO3+O2③2Na2O2+2H2O=4NaOH+O2 ④2NaOH+CO2=Na2CO3+H2O?
反应生成气体产物是O2和H2O(g),
根据方程式,从质量守恒的角度计算.
解答:解:混合物在密闭容器中加热到250℃时,可能发生如下反应:??①2NaHCO3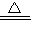 Na2CO3+CO2↑+H2O↑
Na2CO3+CO2↑+H2O↑
②2Na2O2+2CO2=2Na2CO3+O2③2Na2O2+2H2O=4NaOH+O2 ④2NaOH+CO2=Na2CO3+H2O?
反应生成气体产物是O2和H2O(g).
解法一:因为CO2存在,故①×2+②式有?
4NaHCO3+2Na2O2=4Na2CO3+2H2O↑+O2↑⑤?
4 2?
b?a?
2Na2O2+2H2O=4NaOH+O2 ⑥?
2 2?
a-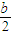
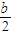 ?
?
根据题意,在⑤式中Na2O2必须过量,则有b>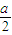 ,所以
,所以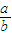 >
> .??
.??
在⑥式中H2O必须过量,则有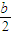 >a-
>a-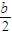 ,
,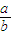 <1,所以
<1,所以 <
<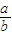 <1.??
<1.??
解法二:依题意可知,残余的固体为Na2CO3和NaOH,生成的气体为O2和H2O(g),则有总反应式为?
bNaHCO3+aNa2O2=bNa2CO3+(2a-b)NaOH+(b-a)H2O+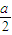 O2?
O2?
所以 2a-b>0,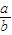 >1/2,b-a>0?
>1/2,b-a>0?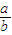 <1.故
<1.故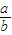 的数值范围:
的数值范围: <
<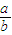 <1.
<1.
只有C符合,在0.5~1之间,
故选C.
点评:本题考查混合物的计算,题目难度中等,注意根据反应的原理结合质量守恒计算.
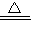 Na2CO3+CO2↑+H2O↑
Na2CO3+CO2↑+H2O↑②2Na2O2+2CO2=2Na2CO3+O2③2Na2O2+2H2O=4NaOH+O2 ④2NaOH+CO2=Na2CO3+H2O?
反应生成气体产物是O2和H2O(g),
根据方程式,从质量守恒的角度计算.
解答:解:混合物在密闭容器中加热到250℃时,可能发生如下反应:??①2NaHCO3
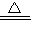 Na2CO3+CO2↑+H2O↑
Na2CO3+CO2↑+H2O↑②2Na2O2+2CO2=2Na2CO3+O2③2Na2O2+2H2O=4NaOH+O2 ④2NaOH+CO2=Na2CO3+H2O?
反应生成气体产物是O2和H2O(g).
解法一:因为CO2存在,故①×2+②式有?
4NaHCO3+2Na2O2=4Na2CO3+2H2O↑+O2↑⑤?
4 2?
b?a?
2Na2O2+2H2O=4NaOH+O2 ⑥?
2 2?
a-
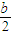
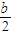 ?
?根据题意,在⑤式中Na2O2必须过量,则有b>
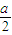 ,所以
,所以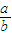 >
> .??
.??在⑥式中H2O必须过量,则有
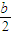 >a-
>a-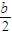 ,
,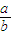 <1,所以
<1,所以 <
<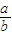 <1.??
<1.??解法二:依题意可知,残余的固体为Na2CO3和NaOH,生成的气体为O2和H2O(g),则有总反应式为?
bNaHCO3+aNa2O2=bNa2CO3+(2a-b)NaOH+(b-a)H2O+
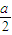 O2?
O2?所以 2a-b>0,
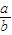 >1/2,b-a>0?
>1/2,b-a>0?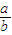 <1.故
<1.故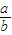 的数值范围:
的数值范围: <
<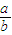 <1.
<1.只有C符合,在0.5~1之间,
故选C.
点评:本题考查混合物的计算,题目难度中等,注意根据反应的原理结合质量守恒计算.

练习册系列答案
相关题目
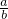 值可能为
值可能为