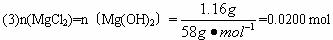题目内容
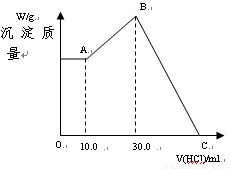
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g白色沉淀,在所得的悬浊液中逐滴加入1 mol·-1L HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示,试回答:
(1)A点沉淀物的化学式为____________;B点沉淀物的化学式为____________。
(2)原混合物中的MgCl2的物质的量为____________,AlCl3的物质的量为____________,NaOH的物质的量为____________。
(3)HCl溶液在C点的加入量是____________。
解析:NaOH、MgCl2、AlCl3溶于水后,将发生反应,若NaOH过量产物将为Mg(OH)2、NaAlO2。向三固体溶于水后所得的悬浊液中滴加盐酸,开始没有沉淀增加,说明混合液中有剩余的NaOH,再滴加盐酸沉淀增加说明AlO2-与H+反应生成了Al(OH)3,当AlO2-完全转化为Al(OH)3后,再加盐酸沉淀[Al(OH)3和 Mg(OH)2]逐渐溶解,直至完全消失。
n(MgCl2)=n[Mg(OH)2]=1.16 g/58 g/mol=0.02 mol;A点→B点发生反应:
AlO2-+H++H2O=Al(OH)3↓,故n(AlCl3)=n(Al3+)=n(H+)=1 mol/L×(30-10)/1000 L=0.02 mol;
反应达B点存在关系式:NaOH~HClMgCl2~2NaOH~Mg(OH)2~2HClAlCl3~4NaOH~
NaAlO2~HCl
故n(HCl)=1 mol/L×(30/1000) L=0.03 mol,n(NaOH)=(10/1000)×1 mol/L+0.02 mol×2+0.02 mol×4=0.13 mol。由B→C还需n(HCl)=3n[Al(OH)3]+2n[Mg(OH)2]=3×0.02 mol+2×0.02 mol=0.10 mol。即还需V(HCl)=0.10 mol/1 mol/L=0.10 L,故V(HCl)=30 mL+100 mL=130 mL。
答案:(1)Mg(OH)2 Mg(OH)2、Al(OH)3
(2)0.02 mol 0.02 mol 0.13 mol
(3)130 mL

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案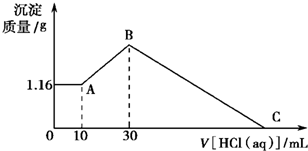 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示,试回答:?
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示,试回答:?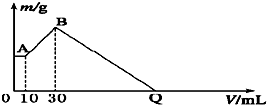 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答: