题目内容
在锌粒与盐酸反应中,改变下列条件不能加快反应速率的是( )
| A、升高反应温度 |
| B、增大盐酸的浓度 |
| C、将小锌粒换成大锌粒 |
| D、在盐酸中滴入几滴CuSO4溶液 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:升高温度、增大酸的浓度、增大固体的接触面积等都可加快化学反应速率,以此来解答.
解答:
解:A、升高反应温度能加快反应速率,故A错误;
B、增大盐酸的浓度能加快反应速率,故B错误;
C、将小锌粒换成大锌粒,即减小单位质量的锌粒的接触面积,不能加快反应速率,故C正确;
D、在盐酸中滴入几滴CuSO4溶液,会形成原电池,加快反应速率,故D错误.
故选C.
B、增大盐酸的浓度能加快反应速率,故B错误;
C、将小锌粒换成大锌粒,即减小单位质量的锌粒的接触面积,不能加快反应速率,故C正确;
D、在盐酸中滴入几滴CuSO4溶液,会形成原电池,加快反应速率,故D错误.
故选C.
点评:本题考查影响化学反应速率的因素,明确常见的外界因素对化学反应速率的影响即可解答,难度不大.

练习册系列答案
相关题目
下列药品置于空气中很容易变质(括号内的物质是变质后的物质),其中是因为氧化还原反应而变质的是( )
| A、Ca(OH)2[CaCO3] |
| B、Fe(OH)3[Fe2O3] |
| C、KI[I2] |
| D、NaOH[Na2CO3] |
几种短周期元素的原子半径及主要化合价如下表
下列说法正确的是( )
| 元素代号 | L | M | X | R | T |
| 原子半径(nm) | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、离子半径大小:r(M3+)>r(T2-) |
| B、R的氧化物对应的水化物不可能具有两性 |
| C、X单质在氧气中燃烧生成XO3 |
| D、L、T形成的简单离子核外电子数相等 |
下列有关化学用语使用正确的是( )
A、硫离子的结构示意图: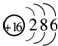 | ||
B、NH4Cl的电子式: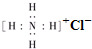 | ||
C、原子核内有10个中子的氧原子:
| ||
| D、水的结构式:H-O-H |
下列有关说法正确的是( )
| A、所有反应都可以用四种基本反应类型进行概括 |
| B、氧化还原反应可能是复分解反应 |
| C、氧化还原反应可能是化合反应,也可能是分解反应 |
| D、置换反应可能不是氧化还原反应 |
 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示,已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2,则线段BC表示
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示,已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2,则线段BC表示