题目内容
【题目】我国钛资源丰富,攀枝花和西昌已探明钛矿储量就有几十亿吨,其重要的矿石有金红石![]() 、钛铁矿
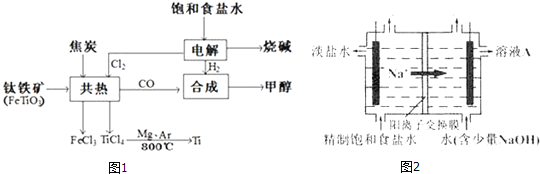
、钛铁矿![]() 以及钒钛铁矿.如图1所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率.
以及钒钛铁矿.如图1所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率.
![]() 常温下为无色液体,具有刺激性气味,极易水解,其化学键类型为 ______ ,写出
常温下为无色液体,具有刺激性气味,极易水解,其化学键类型为 ______ ,写出![]() 水解的方程式 ______
水解的方程式 ______
![]() 写出钛铁矿与焦炭、
写出钛铁矿与焦炭、![]() 共热得到
共热得到![]() 的化学方程式: ______
的化学方程式: ______
![]() ①
① ![]()
②![]()
请写出上图中![]() 生成Ti的热化学反应方程式: ______
生成Ti的热化学反应方程式: ______
![]() 海绵钛可用碘提纯,原理为
海绵钛可用碘提纯,原理为![]()
![]() 下列说法正确的是 ______
下列说法正确的是 ______
A 该反应正反应的![]()
B 在不同温度区域,![]() 的量保持不变
的量保持不变
C 在提纯过程中,![]() 的作用是将粗钛从低温区转移到高温区
的作用是将粗钛从低温区转移到高温区
D 在提纯过程中,![]() 可循环利用
可循环利用
![]() 钛网做阳极电解饱和食盐水常用隔膜电解槽.图2为阳离子交换膜电解槽示意图.
钛网做阳极电解饱和食盐水常用隔膜电解槽.图2为阳离子交换膜电解槽示意图.
①该电解装置阳极在 ______ ![]() 填左室、右室
填左室、右室![]() 氯碱工业电解槽一般采用Ti网作阳极而不用Fe网,其原因是 ______ .
氯碱工业电解槽一般采用Ti网作阳极而不用Fe网,其原因是 ______ .
②右室中加入少量NaOH的原因是 ______ .
![]() 在上述产业链中合成112t甲醇理论上能生产Ti ______
在上述产业链中合成112t甲醇理论上能生产Ti ______ 不考虑生产过程中物质的任何损失
![]()
【答案】极性共价键 ![]()
![]()
![]()
![]()
![]()
![]()
![]() CD 左室 金属钛不易被腐蚀,生产的
CD 左室 金属钛不易被腐蚀,生产的![]() 不会与之反应 增强导电性 56
不会与之反应 增强导电性 56
【解析】
![]() 在常温下是无色液体,应属于分子晶体;
在常温下是无色液体,应属于分子晶体;![]() 水解生成
水解生成![]() 和HCl,依据原子个数守恒写出方程式;
和HCl,依据原子个数守恒写出方程式;
![]() 钛铁矿在高温下与焦炭经氯化得到四氯化钛,还生成氯化铁、CO;
钛铁矿在高温下与焦炭经氯化得到四氯化钛,还生成氯化铁、CO;
![]() 依据热化学方程式和盖斯定律计算得到所需热化学方程式;
依据热化学方程式和盖斯定律计算得到所需热化学方程式;
![]() A. 依据反应类型判断反应的热效应;
A. 依据反应类型判断反应的热效应;
B. 根据温度判断,在不同温度区域,![]() 的量是否发生改变;
的量是否发生改变;
C. 温度不同,反应方程式不同,产物不同;
D. 在提纯过程中,根据反应确定![]() 的量是否变化;
的量是否变化;
![]() 依据溶液中阳离子的移动方向判断电极;金属钛稳定性强于铁,抗氯气的腐蚀能力强于铁;
依据溶液中阳离子的移动方向判断电极;金属钛稳定性强于铁,抗氯气的腐蚀能力强于铁;
![]() 氢氧化钠为强电解质,加入后能够增强电解质溶液的导电能力;
氢氧化钠为强电解质,加入后能够增强电解质溶液的导电能力;
![]() 依据转化关系:
依据转化关系:![]() ,
,![]() ;
;![]() 计算解答。
计算解答。
![]() 在常温下是无色液体,应属于分子晶体,含有的化学键为极性共价键;
在常温下是无色液体,应属于分子晶体,含有的化学键为极性共价键;![]() 水解生成
水解生成![]() 和Cl,化学方程式:
和Cl,化学方程式:![]()
![]()
![]() ;故答案为:极性共价键;
;故答案为:极性共价键;![]()
![]()
![]() ;
;
![]() 钛铁矿在高温下与焦炭经氯化得到四氯化钛,还生成氯化铁、CO,该反应为
钛铁矿在高温下与焦炭经氯化得到四氯化钛,还生成氯化铁、CO,该反应为 ,故答案为:
,故答案为: ;
;
![]()
![]()
由盖斯定律![]() ,得到热化学方程式为:
,得到热化学方程式为:![]() ;故答案为:
;故答案为:![]() ;
;
![]() A. 大多数混合反应是放热反应,该反应的正反应也是放热反应,则该反应正反应的
A. 大多数混合反应是放热反应,该反应的正反应也是放热反应,则该反应正反应的![]() ,故A错误;
,故A错误;
B. 高于![]() ,钛和氯气反应生成四氯化钛,在
,钛和氯气反应生成四氯化钛,在![]() 四氯化钛分解,所以在不同温度区域,
四氯化钛分解,所以在不同温度区域,![]() 的量不同,故B错误;
的量不同,故B错误;
C. 在提纯过程中,高于![]() ,碘和钛反应生成四氯化钛,在
,碘和钛反应生成四氯化钛,在![]() 四氯化钛分解生成碘和钛,所以
四氯化钛分解生成碘和钛,所以![]() 的作用是将粗钛从低温区转移到高温区,故C正确;
的作用是将粗钛从低温区转移到高温区,故C正确;
D. 在提纯过程中,高于![]() ,碘和钛反应生成四氯化钛,在
,碘和钛反应生成四氯化钛,在![]() 四氯化钛分解生成碘和钛,所以
四氯化钛分解生成碘和钛,所以![]() 的量不变,可以循环利用故D正确;
的量不变,可以循环利用故D正确;
故选:CD;
![]() 钠离子为阳离子,电解池中阳离子移向的极为阴极,所以右室为阴极,左室为阳极;金属钛不易被腐蚀,生产的
钠离子为阳离子,电解池中阳离子移向的极为阴极,所以右室为阴极,左室为阳极;金属钛不易被腐蚀,生产的![]() 不会与之反应,抗腐蚀性强与铁,所以氯碱工业电解槽一般采用Ti网作阳极而不用Fe网;故答案为:左室;金属钛不易被腐蚀,生产的
不会与之反应,抗腐蚀性强与铁,所以氯碱工业电解槽一般采用Ti网作阳极而不用Fe网;故答案为:左室;金属钛不易被腐蚀,生产的![]() 不会与之反应;
不会与之反应;
![]() 氢氧化钠为强电解质,加入后能够增强电解质溶液的导电能力;故答案为:增强导电性;
氢氧化钠为强电解质,加入后能够增强电解质溶液的导电能力;故答案为:增强导电性;
![]() 依据转化关系可知:
依据转化关系可知:
![]()
![]()
![]()
112t m
则有![]() ,解得
,解得![]() ,故答案为:56t。
,故答案为:56t。

 金钥匙试卷系列答案
金钥匙试卷系列答案