题目内容
下列各组物质的性质比较,正确的是( )
| A、酸性:H3PO4>H2SO4 |
| B、热稳定性:H2S>H2O |
| C、碱性:Mg(OH)2>NaOH |
| D、氧化性:Cl2>Br2 |
考点:非金属在元素周期表中的位置及其性质递变的规律,金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:A、元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
B、元素的非金属性越强,对应的氢化物越稳定;
C、元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;
D、同一主族元素的单质,从上到下,氧化性逐渐增强.
B、元素的非金属性越强,对应的氢化物越稳定;
C、元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;
D、同一主族元素的单质,从上到下,氧化性逐渐增强.
解答:
解:A、元素的非金属性S>P,所以对应的最高价氧化物的水化物的酸性H3PO4<H2SO4,故A错误;
B、元素的非金属性O>S,对应的氢化物稳定性:H2S<H2O,故B错误;
C、元素的金属性Na>Mg,对应的最高价氧化物的水化物的碱性Mg(OH)2<NaOH,故C错误;
D、同一主族元素的单质,从上到下,氧化性逐渐增强,即Cl2>Br2,故D正确.
故选D.
B、元素的非金属性O>S,对应的氢化物稳定性:H2S<H2O,故B错误;
C、元素的金属性Na>Mg,对应的最高价氧化物的水化物的碱性Mg(OH)2<NaOH,故C错误;
D、同一主族元素的单质,从上到下,氧化性逐渐增强,即Cl2>Br2,故D正确.
故选D.
点评:本题考查较为综合,涉及元素周期律的有关知识,但题目难度不大,注意规律的掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列图象描述正确的是( )
A、 可判断可逆反应A2(g)+3B2(g)?2AB3(g)正反应是放热反应 可判断可逆反应A2(g)+3B2(g)?2AB3(g)正反应是放热反应 |
B、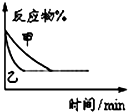 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
C、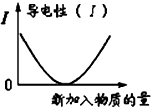 可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
D、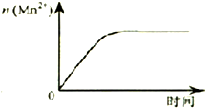 表示10mL 0.01 mol?L-1 KMnO4酸性溶液与过量的0.1mol?L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 表示10mL 0.01 mol?L-1 KMnO4酸性溶液与过量的0.1mol?L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 |
已知0.1mol?L-1的NaHSO4溶液中,c(H+)=0.1mol?L-1,则NaHSO4在水溶液中的电离方程式是( )
| A、NaHSO4=Na++HSO4- |
| B、NaHSO4=Na++H++SO42- |
| C、NaHSO4=Na++H++S6++4O2- |
| D、NaHSO4=NaH2++SO42- |
国家卫生组织宣布,到2000年要消除碘缺乏病,为此食盐必须是国家统一标准的加碘盐,你认为加碘盐的指在食盐(NaCl)中添加适量的( )
| A、碘单质 | B、碘化钠 |
| C、碘酸钾 | D、次碘酸钾 |
在一定条件下,将3mol A和1mol B两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g),2min后该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol?L-1.则下列判断正确的是( )
| A、x=2 |
| B、2min内A的反应速率为0.6 mol?L-1?min-1 |
| C、B的转化率为40% |
| D、若混合气体的密度不变,则表明该反应达到平衡状态 |
下列变化属于物理变化的是( )
| A、石油裂解 |
| B、石油的分馏 |
| C、煤的干馏 |
| D、甲烷和氯气混合后光照 |
用铂作电极电解1L含有0.4molCuSO4和0.2molNaCl的水溶液,一段时间后在一个电极上得到了19.2g Cu,在另一极上析出的气体在标况下的体积是( )
| A、4.48L |
| B、5.6L |
| C、6.72L |
| D、13.44L |
 已知:C(金刚石,固)→C(石墨,固)+1.9kJ,则下列判断正确的是( )
已知:C(金刚石,固)→C(石墨,固)+1.9kJ,则下列判断正确的是( )| A、金刚石转变为石墨的能量的反应进程的关系可用右图表示 |
| B、等质量的石墨比金刚石能量高 |
| C、石墨比金刚石稳定 |
| D、金刚石转化为石墨没有化学键的断裂与生成 |
下列关于元素周期表的说法不正确的是( )
| A、元素周期表中一共有18个纵行 |
| B、原子最外层电子数为2的元素全部位于周期表的第ⅡA族和零族 |
| C、同周期第ⅡA族与第ⅢA族元素的原子序数之差可能为25 |
| D、同主族两种元素的原子序数之差可能为44 |