题目内容
下列图象描述正确的是( )
A、 可判断可逆反应A2(g)+3B2(g)?2AB3(g)正反应是放热反应 可判断可逆反应A2(g)+3B2(g)?2AB3(g)正反应是放热反应 |
B、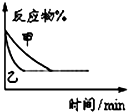 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
C、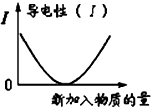 可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
D、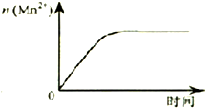 表示10mL 0.01 mol?L-1 KMnO4酸性溶液与过量的0.1mol?L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 表示10mL 0.01 mol?L-1 KMnO4酸性溶液与过量的0.1mol?L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 |
考点:化学反应速率与化学平衡图象的综合应用,体积百分含量随温度、压强变化曲线,电解质溶液的导电性
专题:图示题
分析:A、升高温度,化学平衡向着吸热方向进行,正逆反应速率都增大;
B、增大压强,化学反应速率加快,化学平衡向着气体系数和减小的方向进行;
C、乙酸溶液中通入氨气,开始会生成醋酸铵,随着氨气量的增加,醋酸消耗完毕,导电性会逐渐减弱;
D、KMnO4酸性溶液与H2C2O4溶液的反应是一条自催化反应,即反应生成的锰离子可以作为催化剂.
B、增大压强,化学反应速率加快,化学平衡向着气体系数和减小的方向进行;
C、乙酸溶液中通入氨气,开始会生成醋酸铵,随着氨气量的增加,醋酸消耗完毕,导电性会逐渐减弱;
D、KMnO4酸性溶液与H2C2O4溶液的反应是一条自催化反应,即反应生成的锰离子可以作为催化剂.
解答:
解:A、升高温度,化学平衡向着吸热方向进行,正逆反应速率都增大,根据图象看出是升高温度,反应逆向进行,所以A2(g)+3B2(g)?2AB3(g)正反应是放热反应,故A正确;
B、增大压强,化学反应速率加快,乙的压强大,但是化学平衡向着气体系数和减小的方向即正反应方向进行,反应物的百分含量会减小,故B错误;
C、乙酸溶液中通入氨气,开始会生成醋酸铵,溶液的导电性会增强,故C错误;
D、KMnO4酸性溶液与H2C2O4溶液的反应是一条自催化反应,反应生成的锰离子可以作为催化剂,所以在开始阶段,反应的时间和锰离子的物质的量之间不是正比例关系,故D错误.
故选A.
B、增大压强,化学反应速率加快,乙的压强大,但是化学平衡向着气体系数和减小的方向即正反应方向进行,反应物的百分含量会减小,故B错误;
C、乙酸溶液中通入氨气,开始会生成醋酸铵,溶液的导电性会增强,故C错误;
D、KMnO4酸性溶液与H2C2O4溶液的反应是一条自催化反应,反应生成的锰离子可以作为催化剂,所以在开始阶段,反应的时间和锰离子的物质的量之间不是正比例关系,故D错误.
故选A.
点评:本题结合图象题考查化学反应速率和平衡移动的影响因素以及溶液的导电性情况知识,注意知识的归纳和整理是关键,难度不大.

练习册系列答案
 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
在无色透明的酸性溶液中,能大量共存的离子组是( )
| A、Al3+、Na+、Cl-、SO42- |
| B、Cu2+、Ca2+、CO32-、Cl- |
| C、NH4+、Ba2+、NO3-、HCO3- |
| D、K+、Fe3+、Cl-、NO3- |
下列说法或表示方法正确的是( )
A、丙烷分子的比例模型: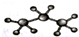 |
| B、乙醚的分子式为:C2H6O |
C、2-乙基-1,3-丁二烯分子的键线式: |
| D、化学名词:乙酸乙脂、苯、活性碳、钳锅 |
下列溶液中Cl-的物质的量浓度与50mL 1mol/L AlCl3溶液中Cl-物质的量浓度相等的是( )
| A、150mL 2mol/L KCl溶液 |
| B、75mL 1.5mol/L MgCl2溶液 |
| C、100mL 1mol/L NaCl溶液 |
| D、25mL 2mol/L AlCl3溶液 |
根据下表中烃的分子式排列规律,空格中烃的同分异构体中一氯代物种数不可能是( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
| A、1种 | B、2种 | C、3种 | D、4种 |
A、B、C均为短周期元素,它们在周期表中的位置如图所示.B、C两元素原子序数之和为A元素原子序数的4倍,则A、B、C依次是( )
| A | ||
| B | C |
| A、C、Al、P |
| B、N、Si、S |
| C、O、P、Cl |
| D、F、S、Ar |
下列各组物质的性质比较,正确的是( )
| A、酸性:H3PO4>H2SO4 |
| B、热稳定性:H2S>H2O |
| C、碱性:Mg(OH)2>NaOH |
| D、氧化性:Cl2>Br2 |