题目内容
下列氢氧化物中,碱性最强的是( )
| A、Mg(OH)2 |
| B、NaOH |
| C、RbOH |
| D、Al(OH)3 |
考点:同一周期内元素性质的递变规律与原子结构的关系,同一主族内元素性质递变规律与原子结构的关系
专题:
分析:根据金属性越强,最高价氧化物的水化物的碱性越强,以此来解答.
解答:
解:Na、Mg、Al在同一周期,从左到右金属性减弱,所以金属性Na>Mg>Al,
而Na、Rb在同一主族,由同主族从上到下金属性在增强,
则金属性Rb>Na,综上所述金属性:Rb>Na>Mg>Al,
金属性越强,最高价氧化物的水化物的碱性越强,
显然RbOH的碱性最强,
故选C.
而Na、Rb在同一主族,由同主族从上到下金属性在增强,
则金属性Rb>Na,综上所述金属性:Rb>Na>Mg>Al,
金属性越强,最高价氧化物的水化物的碱性越强,
显然RbOH的碱性最强,
故选C.
点评:本题考查元素周期律,明确金属性强弱是解答本题的关系,熟悉元素周期律即可解答,难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
下列有机物结构简式书写错误的是( )
| A、CH3(CH2)3CH3 |
| B、CH3C(CH3)2CH2CH3 |
| C、CH3(CH2)2C(CH3)3 |
| D、CH3CH(CH3)3CH2CH3 |

 A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题.
A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题.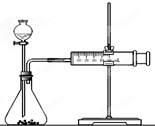 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.