题目内容
15.化学与生产、生活密切相关.下列说法正确的是( )| A. | 砒霜的主要成分是三硫化二砷 | |
| B. | 水分子间的氢键是一种特殊的化学键 | |
| C. | 过量服用阿司匹林引起酸中毒后,可用静脉注射NaHCO3溶液的方法解毒 | |
| D. | 铜单质制成的“纳米铜”在空气中能燃烧,说明“纳米铜”的金属性比铜片强 |
分析 A.砒霜为剧毒物质,主要成分是三氧化二砷(As2O3);
B.氢键不属于化学键,是分子间作用力一种;
C.阿司匹林为常用的感冒用药,过量服用会造成酸中毒;
D.铜片在空气中难燃烧,纳米级铜粉在空气中易燃烧,是由于与氧气的接触面积不同.
解答 解:A.砒霜的主要成分是三硫化二砷,故A正确;
B.水分子间的氢键不是一种特殊的化学键,是分子间作用力一种,故B错误;
C.阿司匹林为感冒用药,但因其含有水杨酸,服用过量易造成酸中毒,可静脉注射NaHCO3来降低酸性,故C正确;
D.铜片在空气中难燃烧,纳米级铜粉在空气中易燃烧,是由于与氧气的接触面积不同,不能说明“纳米铜”的金属性比铜片强,故D错误;
故选:AC.
点评 本题考查了物质的组成与性质,涉及砒霜的成分、纳米铜、水杨酸的性质,氢键与化学键的区别,解题时注意抓住化学键是分子内、原子间的作用力,题目难度不大.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
4.某溶液只含下表离子中的几种,且各离子的物质的量浓度相等(不考虑水的电离与离子水解).
某同学进行了如下实验(必要时可加热):

下列说法正确的是( )
| 阳离子 | K+、NH4+、Fe2+、Mg2+、Cu2+ |
| 阴离子 | OH-、Cl-、CO32-、SO42- |

下列说法正确的是( )
| A. | 滤液A中可能含有K+ | |
| B. | 沉淀B中一定含有Mg(OH)2 | |
| C. | 由沉淀A推断原溶液中一定含有SO42- | |
| D. | 原溶液中只含有NH4+、Fe2+、Cl-、SO42- |
6.某有机物的结构简式为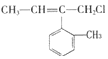 ,则该物质不能发生的反应有( )
,则该物质不能发生的反应有( )
 ,则该物质不能发生的反应有( )
,则该物质不能发生的反应有( )| A. | 加成反应 | B. | 氧化反应 | C. | 取代反应 | D. | 消去反应 |
3.设NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 18 gD2O含电子数目为10NA | |
| B. | 1 L 0.1 mol/L NH4NO3溶液中含有氮原子数目为0.2 NA | |
| C. | 0.1 mol CaC2固体含离子数目为0.3 NA | |
| D. | agC2H4和C3H6混合气体含原予数目为aNA/14 |
10. 科学家首次从人尿中分离出具有生长素效应的化学物 质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )
科学家首次从人尿中分离出具有生长素效应的化学物 质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )
 科学家首次从人尿中分离出具有生长素效应的化学物 质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )
科学家首次从人尿中分离出具有生长素效应的化学物 质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )| A. | 吲哚乙酸不能使酸性高锰酸钾褪色 | |
| B. | 吲哚乙酸可以发生取代反应、加成反应、氧化反应,不可以发生还原反应 | |
| C. | 1 mol吲哚乙酸与足量氢气发生加成反应时,可以消耗5 mol H2 | |
| D. | 吲哚乙酸苯环上的二氯代物共有六种结构 |
20.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,6.0g NO和2.24L O2混合,所得气体的分子数目为0.2NA | |
| B. | 常温常压下,0.1mol Na2O和Na2O2组成的混合物中,阴离子的数目为0.1NA | |
| C. | C2H4和C3H6的混合物的质量为mg,所含碳氢键的数目为$\frac{3m}{14}$NA | |
| D. | 1mol甲基( )所含的电子数为7NA )所含的电子数为7NA |
2.下列关于化学键的有关说法不正确的是( )
| A. | 氢键不是化学键 | |
| B. | 非极性共价键只能存在于单质中 | |
| C. | 含有共价键的化合物不一定是共价化合物 | |
| D. | 含有离子键的化合物一定是离子化合物 |