题目内容
15.在固定体积的密闭容器中加入4mol A和2mol B发生如下反应2A(g)+B(g)?3C(g)+D(g)达到平衡时C的浓度为m mol/L,若温度不变时按下列4种配比作为起始物质,达到平衡后C浓度仍为m mol/L的是( )| A. | 2molA+1molB | B. | 2molA+1molB+3molC+1mol D | ||
| C. | 3molC+1molD | D. | 4molA+2molB+3molC |
分析 恒温恒容下,不同途径达到平衡后,C的浓度仍为W mol/L,说明与原平衡为等效平衡,按化学计量数转化到左边,满足n(A)=4mol,n(B)=2mol即可,据此解答.
解答 解:2A(g)+B(g)  3C(g)+D(g)
3C(g)+D(g)
4mol 2mol 6mol 2mol
A、2molA+1molB与4molA+2molB不相等,在温度、体积不变的情况下不是相同平衡状态,故A错误;
B、开始加入2molA+1molB+3molC+1molD,按化学计量数转化到左边可得4molA、2molB,与原平衡为等效平衡,故B正确;
C、3molC+1molD相当于2molA+1molB,与4molA+2molB不相等,在温度、体积不变的情况下不是相同平衡状态,故C错误;
D、4molA+2molB+3molC与4molA+2molB不相等,在温度、体积不变的情况下不是相同平衡状态,故D错误.
故选B.
点评 本题考查化学平衡的有关计算、等效平衡,难度中等,构建平衡建立的途径是解题关键.

练习册系列答案
相关题目
10.在一定条件下,反应2HI(g)?H2(g)+I2(g)(紫红色)△H>0,达到平衡时,要使混合气体的颜色加深,可采取的措施是( )
①增大氢气的浓度
②升高温度
③降低温度
④缩小体积
⑤增大HI的浓度
⑥减小压强.
①增大氢气的浓度
②升高温度
③降低温度
④缩小体积
⑤增大HI的浓度
⑥减小压强.
| A. | ①③⑥ | B. | ②④⑤ | C. | ③⑤⑥ | D. | ①③⑤ |
7.下列叙述一定正确的是( )
| A. | 将wg a%的NaCl溶液蒸发掉w/2g水,得到2a%的NaCl溶液 | |
| B. | 将25g无水CuSO4溶于水制成100mL溶液,其浓度为1mol/L | |
| C. | 将1体积c1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2c1mol/L | |
| D. | 将5.85gNaCl晶体溶入100mL水中,制得0.1mol/L的NaCl溶液 |


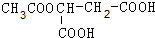 +H2O.
+H2O.