题目内容
用NA表示阿伏加德罗常数的值.下列叙述正确的是
- A.0.1 mol癸烷分子中,共价键数为3 NA
- B.1 mol乙醇在O2中完全燃烧,电子转移数目为6 NA
- C.标准状况下,22.4 L甲醇中含有的氧原子数为1.0 NA
- D.室温下,26.0 g乙炔和苯乙烯的混合物中含有的碳原子数目为2NA
D
分析:A.癸烷分子为C10H22,分子含有共价键数目为31,据此计算共价键物质的量,再根据N=nNA计算共价键数目;
B.计算消耗的氧气的物质的量,反应中氧元素由0价计算为-2价,据此计算转移电子物质的量,再根据N=nNA计算转移电子数目;
C.标准状况下,甲醇是液体;
D.乙炔与苯乙烯的最简式为CH,计算最简式的物质的量,再根据N=nNA计算碳原子数目.
解答:A.癸烷分子为C10H22,分子含有共价键数目为31,0.1mol癸烷含有共价键物质的量为0.1mol×31=3.1mol,故含有共价键数目为3.1mol×NAmol-1=3.1NA,故A错误;
B.1 mol乙醇在O2中完全燃烧,消耗的氧气的物质的量为(2+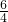 -
- )mol=3mol,反应中氧元素由0价计算为-2价,故转移电子物质的量为3mol×2×2=12mol,故转移电子数目为12mol×NAmol-1=12NA,故C错误;
)mol=3mol,反应中氧元素由0价计算为-2价,故转移电子物质的量为3mol×2×2=12mol,故转移电子数目为12mol×NAmol-1=12NA,故C错误;
C.标准状况下,甲醇是液体,不能利用气体摩尔体积计算其物质的量,故C错误;
D.乙炔与苯乙烯的最简式为CH,26.0 g乙炔和苯乙烯的混合物,最简式的物质的量为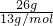 =2mol,故含有碳原子数目为2mol×NAmol-1=2NA,故D正确;
=2mol,故含有碳原子数目为2mol×NAmol-1=2NA,故D正确;
故选D.
点评:本题考查常用化学计量的有关计算,难度不大,D选项可以先利用质量分数计算碳原子的质量,再进行计算.
分析:A.癸烷分子为C10H22,分子含有共价键数目为31,据此计算共价键物质的量,再根据N=nNA计算共价键数目;
B.计算消耗的氧气的物质的量,反应中氧元素由0价计算为-2价,据此计算转移电子物质的量,再根据N=nNA计算转移电子数目;
C.标准状况下,甲醇是液体;
D.乙炔与苯乙烯的最简式为CH,计算最简式的物质的量,再根据N=nNA计算碳原子数目.
解答:A.癸烷分子为C10H22,分子含有共价键数目为31,0.1mol癸烷含有共价键物质的量为0.1mol×31=3.1mol,故含有共价键数目为3.1mol×NAmol-1=3.1NA,故A错误;
B.1 mol乙醇在O2中完全燃烧,消耗的氧气的物质的量为(2+
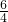 -
- )mol=3mol,反应中氧元素由0价计算为-2价,故转移电子物质的量为3mol×2×2=12mol,故转移电子数目为12mol×NAmol-1=12NA,故C错误;
)mol=3mol,反应中氧元素由0价计算为-2价,故转移电子物质的量为3mol×2×2=12mol,故转移电子数目为12mol×NAmol-1=12NA,故C错误;C.标准状况下,甲醇是液体,不能利用气体摩尔体积计算其物质的量,故C错误;
D.乙炔与苯乙烯的最简式为CH,26.0 g乙炔和苯乙烯的混合物,最简式的物质的量为
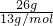 =2mol,故含有碳原子数目为2mol×NAmol-1=2NA,故D正确;
=2mol,故含有碳原子数目为2mol×NAmol-1=2NA,故D正确;故选D.
点评:本题考查常用化学计量的有关计算,难度不大,D选项可以先利用质量分数计算碳原子的质量,再进行计算.

练习册系列答案
相关题目