题目内容
16.下列说法或表示方法中正确的是( )| A. | 等质量的硫蒸气和硫固体分别完全燃烧,反应的热效应△H1>△H2 | |
| B. | 由C(石墨)═C(金刚石);△H=+1.9KJ/mol,可知1mol石墨的总键能比1mol金刚石的总键能大1.9kJ,即金刚石比石墨稳定 | |
| C. | 在101KPa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=+285.8KJ/mol | |
| D. | 放热及熵增加的反应,一定能自发进行 |
分析 A.根据气体变成固体放热判断;
B.石墨能量比金刚石小,能量越低越稳定;
C.反应放热,△H<0;
D.△H-T•△S<0反应自发.
解答 解:A.固体硫变为硫蒸汽要吸热,所以固体硫燃烧时放出的热量较少,则等质量的硫蒸气和硫固体分别完全燃烧,反应的热效应△H1<△H2,故A错误;
B.由C(石墨)→C(金刚石);△H=+1.9KJ/mol,可知反应为吸热反应,则石墨能量比金刚石小,能量越低越稳定,所以石墨比金刚石稳定,故B错误;
C.氢气的燃烧反应为放热反应,所以△H=-285.8kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=-285.8KJ/mol,故C错误;
D.放热及熵增加,△H-T•△S<0反应自发,故D正确;
故选D.
点评 本题考查反应热与焓变,注意相关基础知识的积累,注意把握问题的角度,理解物质的聚集状态与能量的关系、稳定的大小比较等问题.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
6.下列离子方程式方程式中正确的是( )
| A. | NaHCO3溶液中HCO3-水解:HCO3-+H2O?H2CO3+OH- | |
| B. | AlCl3溶液中Al3+水解:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | NaHS溶液中HS-水解:HS-+H2O?H3O++S2- | |
| D. | 碳酸溶液中H2CO3的电离:H2CO3?2H++CO32- |
4.下列各组离子一定能大量共存的是( )
| A. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 在强碱溶液中:Na+、K+、AlO2-、CO32- | |
| C. | 在c(H+)=1×10-13mol/L的溶液中:NH4+、Al3+、SO42-、HCO3- | |
| D. | 在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
11.目前出现的元素周期表不少于700种,有平面形、环形、塔形、扇形、台阶形、三角式、透视式、环式、“8”式,等等.这些周期表有的对称美妙,有的奇异专业…下列有关现在的长式周期表的判断中正确的是( )
| A. | 从左往右数第七纵行是第ⅦA族 | |
| B. | 所含元素种类最多的周期是第六周期 | |
| C. | 第IA族的全部元素是金属元素 | |
| D. | 第ⅥA族的全部元素只能表现出非金属的性质 |
1.根据如图提供的信息,下列所得结论不正确的是( )
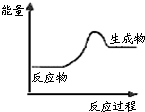

| A. | 该反应为放热反应 | |
| B. | 该反应一定有能量转化成了化学能 | |
| C. | 反应物比生成物稳定 | |
| D. | 因为反应物的总能量低于生成物的总能量,所以该反应需要加热才能发生 |
6.强酸性溶液X中可能含有Na+、K+、NH4+、Fe2+、A13+、CO32-、SO32-、SO42-、C1-中的若干种,某同学为了确认其成分,取X溶液进行连续实验,实验过程及产物如下:

下列结论正确的是( )

下列结论正确的是( )
| A. | X中肯定存在Na+、Fe2+、A13+、NH4+、SO42- | |
| B. | 气体F在氧气中经催化氧化可生成气体A | |
| C. | 沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀I一定是Al(OH )3 | |
| D. | X中不能确定的离子是Fe2+、SO32-、K+和C1- |
3.在一密闭容器中,反应aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积扩大到原体积的2倍,达到新的平衡后,B的浓度是原来的0.6倍,则下列叙述不正确的是( )
| A. | 平衡向正反应方向移动 | B. | 物质A的转化率增大 | ||
| C. | 物质B的质量分数增加 | D. | a>b |
4.根据等电子原理,下列各组分子或离子的空间构型不相似的是( )
| A. | SO2和O3 | B. | CO2和H2O | C. | NH4+和CH4 | D. | H3O+和NH3 |