题目内容
 右图是一个化学过程的示意图.已知甲池的总反应式为:
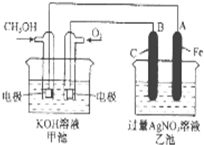
右图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O
(1)请回答下列电极的名称:通入CH3OH的电极名称是
(2)写出电极反应式:通入O2的电极的电极反应式是
(3)乙池中反应的化学方程为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:燃料电池中,通入燃料的电极为负极,电极反应为CH3OH-6e-+2OH-=CO32-+3H2O,通入氧化剂的电极为正极,正极反应为O2+4e-+2H2O=4OH-,B是阳极、A是阴极,阳极、阴极电极反应分别为4OH--4e-=O2↑+2H2O、Ag++e-=Ag,据此分析解答.
解答:
解:(1)燃料电池中,燃料失电子发生氧化反应,所以通入燃料甲醇的电极是负极,通入氧气的电极为正极,则B电解为阳极、A为阴极,故答案为:负极;阳极;
(2)通入氧气的电极上得电子发生还原反应,所以为正极,电极反应为O2+4e-+2H2O=4OH-,A电极上银离子放电生成银,电极反应为Ag++e-=Ag,
故答案为:O2+4e-+2H2O=4OH-;Ag++e-=Ag;
(3)乙池中,C电极上氢氧根离子放电、Fe电极上银离子放电,所以电池反应式为4AgNO3+2H2O
4Ag+4HNO3+O2↑,
故答案为:4AgNO3+2H2O
4Ag+4HNO3+O2↑.
(2)通入氧气的电极上得电子发生还原反应,所以为正极,电极反应为O2+4e-+2H2O=4OH-,A电极上银离子放电生成银,电极反应为Ag++e-=Ag,
故答案为:O2+4e-+2H2O=4OH-;Ag++e-=Ag;
(3)乙池中,C电极上氢氧根离子放电、Fe电极上银离子放电,所以电池反应式为4AgNO3+2H2O
| ||
故答案为:4AgNO3+2H2O
| ||
点评:本题考查了原电池和电解池原理,根据得失电子确定正负极,再结合离子放电顺序确定阴阳极上发生的反应,难点是电极反应式的书写.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列叙述正确的是( )
| A、常温常压下,4.6g NO2气体约含有1.81×1023个原子 |
| B、在标准状况下,80g SO3所占的体积约为22.4L |
| C、常温下,0.1mol?L-1醋酸溶液的pH约为1 |
| D、标准状况下,22.4L氯气与足量氢氧化钠溶液反应,转移的电子数为2NA |
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法错误的是( )


| A、溶液中H+向负极移动 |
| B、电子由Zn经外电路流向Cu |
| C、Zn电极反应:Zn-2e-=Zn2+ |
| D、Cu是正极 |


 ,合成路线如下
,合成路线如下
