题目内容
利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍。
反应一:Ni(粗,s)+4CO(g)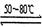 Ni(CO)4(g) ΔH < 0
Ni(CO)4(g) ΔH < 0
反应二:Ni(CO)4(g)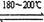 Ni(纯,s)+4CO(g) ΔH > 0
Ni(纯,s)+4CO(g) ΔH > 0
下列说法错误的是
| A.对于反应一,适当增大压强,有利于Ni(CO)4的生成 |
| B.提纯过程中,CO气体可循环使用 |
| C.升高温度,反应一的反应速率减小,反应二的速率增大 |
| D.对反应二,在180—200℃,温度越高,Ni(CO)4(g)的转化率越高 |
C
解析试题分析:A反应一增大压强,向正向移动,正确。B中一氧化碳气体可以循环利用,正确。C中升高温度,速率增大,C错误。D反应二中温度越高,由于反应吸热,向正向移动,转化率增大。正确。
考点:化学反应平衡原理
点评:本题考查了温度,压强对反应平衡的作用,考点比较简单。

练习册系列答案
相关题目
利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍.Ni(s)+4CO(g)
Ni(CO)4(g)△H<0,下列说法正确的是( )
| 50-80℃ |
| 180-200℃ |
| A、50~80℃时,适当增大压强,有利于Ni(CO)4的生成 | ||
| B、利用上述原理提纯粗镍需要消耗大量的CO气体 | ||
| C、50~200℃范围内,该反应的平衡常数随温度的升高而减小 | ||
D、该反应的平衡常数表达式是K=
|
 Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H
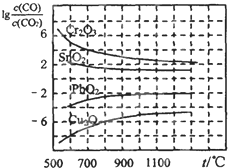 一氧化碳是一种用途相当广泛的化工基础原料.
一氧化碳是一种用途相当广泛的化工基础原料. Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H