题目内容
为提纯下列物质(括号内为少量杂质),所选用的除杂式试剂和分离方法正确的是( )
| 提纯物质 | 除杂试剂 | 分离法 | |
| A | KCl溶液(FeCl3) | 氨水 | 过滤 |
| B | 乙酸乙酯(乙酸) | 乙醇和浓硫酸 | 分液 |
| C | Fe粉(Al粉) | NaOH溶液 | 过滤 |
| D | 乙醇(H2O) | 金属钠 | 蒸馏 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯和除杂
专题:化学实验基本操作
分析:根据除杂质至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质,以此来解答.
A.FeCl3和NaOH溶液反应生成氢氧化铁沉淀和氯化钠,引入新杂质;
B.乙醇和乙酸的反应在浓硫酸的条件下发生,且反应是可逆反应;
C.铝能与氢氧化钠反应;
D.乙醇和水都和钠发生反应.
A.FeCl3和NaOH溶液反应生成氢氧化铁沉淀和氯化钠,引入新杂质;
B.乙醇和乙酸的反应在浓硫酸的条件下发生,且反应是可逆反应;
C.铝能与氢氧化钠反应;
D.乙醇和水都和钠发生反应.
解答:
解:A.氯化铁与NaOH溶液反应生成氢氧化铁沉淀和氯化钠,NH4Cl溶液和NaOH溶液反应生成氨水和氯化钠,不符合除杂的原理,正确的方法是加入适量氢氧化钾后过滤,故A错误;
B.乙醇和乙酸的反应必须在浓硫酸的条件下发生,且反应是可逆反应,不符合除杂的原理,可以用饱和碳酸钠溶液除去,故B错误;
C.铝能与氢氧化钠反应,而铁不能,可以实现除杂,故C正确;
D.乙醇和水都和钠发生反应,不能除去水,可选用先加生石灰,再用蒸馏的方法除去混杂在乙醇中的少量水,故D错误;
故选C.
B.乙醇和乙酸的反应必须在浓硫酸的条件下发生,且反应是可逆反应,不符合除杂的原理,可以用饱和碳酸钠溶液除去,故B错误;
C.铝能与氢氧化钠反应,而铁不能,可以实现除杂,故C正确;
D.乙醇和水都和钠发生反应,不能除去水,可选用先加生石灰,再用蒸馏的方法除去混杂在乙醇中的少量水,故D错误;
故选C.
点评:本题考查物质的分离、提纯,侧重于学生的分析能力、实验能力和评价能力的考查,难度不大,注意把握物质的性质的异同,注意除杂时不能引入新的杂质.

练习册系列答案
相关题目
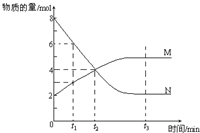 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:2 N?M |
| B、t2时,正逆反应速率相等,达到平衡 |
| C、t3时,正反应速率大于逆反应速率 |
| D、t1时,N的浓度是M浓度的2倍 |
下列有关实验的叙述,正确的是( )
| A、用NaOH溶液除去乙酸乙酯中混有的乙酸、乙醇,然后分液 |
| B、分馏石油时,温度计的末端必须插入液面下 |
| C、用分液漏斗分离环己烷和水的混合液体 |
| D、用浓氨水洗涤做过银镜反应的试管 |
| E、配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加到沉淀刚好溶解为止 |
| F、蔗糖水解后,直接滴加新制氢氧化铜悬浊液并加热检验水解产物中的葡萄糖 |
有甲、乙、丙、丁四个集气瓶中分别盛有H2、Cl2、HCl、HBr中任意一种气体.若将甲和丙两气体混合,见光爆炸.若将丙、丁两气体混合后,瓶壁上出现深红棕色的液滴.则乙气体是( )
| A、H2 |
| B、Cl2 |
| C、HCl |
| D、HBr |
新型塑料膜材料ETFE[名称为聚氟乙烯,化学式(C2H2F2)n],美观、耐用,可以使用15至20年.以下关于聚氟乙烯的说法不正确的是( )
| A、聚氟乙烯属于有机物 |
| B、聚氟乙烯是加聚反应的产物 |
| C、聚氟乙烯溶于水,易与空气中的氧气反应 |
| D、聚氟乙烯中碳元素的质量分数为37.5% |
关于有机物 的叙述错误的是( )
的叙述错误的是( )
 的叙述错误的是( )
的叙述错误的是( )| A、分子式为C6H8O |
| B、含有羟基 |
| C、含有甲基 |
| D、含有苯环结构 |
