题目内容
15.下列反应的离子方程式中,书写正确的是( )| A. | 实验室用大理石跟稀盐酸制取二氧化碳2H++CO32-═CO2↑+H2O | |
| B. | 氯气与水反应 Cl2+H2O═2H++Cl-+ClO- | |
| C. | 氧化铝跟氢氧化钠溶液反应Al2O3+OH-═AlO2-+H2O | |
| D. | 金属钠跟水反应2Na+2H2O═2Na++2OH-+H2↑ |
分析 A.碳酸钙为难溶物,离子方程式中碳酸钙不能拆开;
B.次氯酸为弱酸,离子方程式中次氯酸不能拆开;
C.离子方程式两边Al、H元素不守恒,违反了质量守恒定律;
D.钠与水反应生成氢氧化钠和氢气.
解答 解:A.大理石的主要成分为碳酸钙,碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故A错误;
B.氯气与水反应生成氯化氢好次氯酸,次氯酸为弱酸,需要保留分子式,正确的离子方程式为:Cl2+H2O═H++Cl-+HClO,故B错误;
C.氧化铝跟氢氧化钠溶液反应生成偏铝酸钠和水,正确的离子方程式为:Al2O3+2OH-═2AlO2-+H2O,故C错误;
D.钠跟水反应的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度中等,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
相关题目
7.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 含有2NA个氧原子的氧气与臭氧的混合气体的质量为16g | |
| B. | 标准状况下,22.4 mL水中含有的分子数目约为1.24NA | |
| C. | 300 mL 2 mol•L-1酒精溶液中所含分子数为0.6 NA | |
| D. | 1 mol Cl2参加的任何反应转移电子数都是2NA |
3.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,48g O3含有的分子数为NA | |
| B. | 1molNa2O2晶体中阴离子数为2 NA | |
| C. | 标准状况下,33.6L的 四氯化碳(CCl4)中含有的碳原子数目为1.5NA | |
| D. | 常温常压下,7.1 g Cl2与足量的Fe充分反应,转移的电子数目为0.3 NA |
4.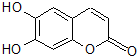 中草药秦皮中含有的七叶树内酯(如图)具有抗菌作用.若1mol该物质分别与浓溴水和H2完全反应,则消耗的Br2和H2的物质的量最多分别为( )
中草药秦皮中含有的七叶树内酯(如图)具有抗菌作用.若1mol该物质分别与浓溴水和H2完全反应,则消耗的Br2和H2的物质的量最多分别为( )
 中草药秦皮中含有的七叶树内酯(如图)具有抗菌作用.若1mol该物质分别与浓溴水和H2完全反应,则消耗的Br2和H2的物质的量最多分别为( )
中草药秦皮中含有的七叶树内酯(如图)具有抗菌作用.若1mol该物质分别与浓溴水和H2完全反应,则消耗的Br2和H2的物质的量最多分别为( )| A. | 2molBr2 3molH2 | B. | 2molBr2 4molH2 | C. | 3molBr2 4molH2 | D. | 3molBr2 5molH2 |
5.下列仪器中一般不用作反应容器的是( )
| A. | 试管 | B. | 烧瓶 | C. | 量筒 | D. | 烧杯 |
 .
.