题目内容
18.在一密闭气缸中,用一不漏气可滑动的活塞隔开,左边充有N2,右边充有H2和O2的混合气体,在20℃时,将右边混合气体点燃,反应后冷却到原来温度,若活塞原来离气缸左端的距离为总长的$\frac{1}{4}$,反应后静止于气缸的正中(忽略水蒸气),则原来H2和O2的体积比为4:5、7:2.分析 左室中氮气的物质的量不变,令开始氮气的物质的量为1mol,左右两室压强相同,体积之比等于物质的量之比,据此计算开始右室中氢气与氧气的物质的量,反应后左右体积相等,则右室剩余气体的物质的量为1mol,该气体可能是氧气或氢气,根据差量法计算,原混合气体中氢气、氧气的物质的量,进而计算体积比.
解答 解:左室中氮气的物质的量不变,令开始氮气的物质的量为1mol,左右两室压强相同,体积之比等于物质的量之比,故开始右室中氢气与氧气的物质的量为1mol×$\frac{\frac{3}{4}}{\frac{1}{4}}$=3mol,反应后左右体积相等,则右室剩余气体的物质的量为1mol,则:
2H2+O2=2H2O 气体物质的量减少△n
2 1 3
$\frac{4}{3}$mol $\frac{2}{3}$mol 3mol-1mol=2mol
若剩余气体为氢气,则原混合气体中氧气为$\frac{2}{3}$mol,则氢气为3mol-$\frac{2}{3}$mol=$\frac{7}{3}$mol,H2和O2的体积比为$\frac{7}{3}$mol:$\frac{2}{3}$mol=7:2,
若剩余气体是氧气,则原混合气体中氢气为$\frac{4}{3}$mol,则氢气为3mol-$\frac{4}{3}$mol=$\frac{5}{3}$mol,H2和O2的体积比为$\frac{4}{3}$mol:$\frac{5}{3}$mol=4:5,
故答案为:4:5、7:2.
点评 本题考查化学计算、阿伏伽德罗定律等,难度中等,根据左室氮气的物质的量利用体积判断右室气体的物质的量是关键.

练习册系列答案
相关题目
17.在恒温、体积为2L的密闭容器中进行反应:2A(g)?3B(g)+C(g),若反应物在前20s由3mol将为1.8mol,则前20s的平均反应速率为( )
| A. | v(B)=0.03mol•L-1•s-1 | B. | v(B)=0.045mol•L-1•s-1 | ||
| C. | v(C)=0.03mol•L-1•s-1 | D. | v(C)=0.06mol•L-1•s-1 |
18.下列说法正确的是( )
| A. | 软脂酸和油酸互为同系物 | |
| B. |  的命名为:3-甲基-2-丁醇 的命名为:3-甲基-2-丁醇 | |
| C. | 苯酚能与溴水反应,苯不能与溴水反应,说明羟基对苯环有影响 | |
| D. | 与 互为同分异构体的芳香族化合物有4种 互为同分异构体的芳香族化合物有4种 |
6.将等质量的四块铜片在酒精灯上加热后,分别插入下列溶液中,放置片刻后铜片质量与加热前相同的是( )
| A. | 硝酸 | B. | 盐酸 | C. | 石灰水 | D. | 乙醇 |
13.某实验小组用0.50mol/L NaOH溶液和0.50mol/L H2SO4溶液进行中和热的测定.
Ⅰ.配制 0.50mol/L NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,配制溶液需要用250ml容量瓶,则至少需要称量NaOH固体5.0g.
(2)从下图中选择称量NaOH固体所需要的仪器(填序号)a b e.
Ⅱ.测定中和热的实验装置如图所示
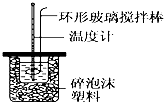
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol):NaOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol.
(2)取50mL NaOH溶液和30mL硫酸进行实验,实验数据如表.
①请填写下表中平均温度差的空格:
②近似认为0.50mol/L NaOH溶液和0.50mol/L H2SO4溶液的密度都是1g/cm3,中和后生成溶液的比热容
c=4.18J/(g•℃).则中和热△H=-53.5kJ/mol(保留小数点后一位).
③上述实验结果的数值与57.3kJ/mol有偏差,产生偏差的原因可能是(填序号)acd.
a.实验装置保温、隔热效果差
b.在量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
④已知强酸与强碱在稀溶液里反应的中和热可表示为
H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1对下列反应:
CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-Q1 kJ•mol-1
$\frac{1}{2}$H2SO4(浓)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-Q2 kJ•mol-1
HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l)△H=-Q3 kJ•mol-1
上述反应均在溶液中进行,则下列Q1、Q2、Q3的关系正确的是A
A.Q2>Q3>Q1 B.Q2>Q1>Q3 C.Q1=Q2=Q3 D.Q2=Q3>Q1.
Ⅰ.配制 0.50mol/L NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,配制溶液需要用250ml容量瓶,则至少需要称量NaOH固体5.0g.
(2)从下图中选择称量NaOH固体所需要的仪器(填序号)a b e.
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 | 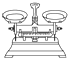 | 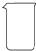 |  |  |  |  |
| 序号 | a | b | c | d | e | f |

(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol):NaOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol.
(2)取50mL NaOH溶液和30mL硫酸进行实验,实验数据如表.
①请填写下表中平均温度差的空格:
| 温度 实验次数 | 起始温度t1/℃ | 终止温 度t2/℃ | 平均温度差 (t2-t1)/℃ | ||
| H2SO4溶液 | NaOH溶液 | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 请填写(4.0℃ ) |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
c=4.18J/(g•℃).则中和热△H=-53.5kJ/mol(保留小数点后一位).
③上述实验结果的数值与57.3kJ/mol有偏差,产生偏差的原因可能是(填序号)acd.
a.实验装置保温、隔热效果差
b.在量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
④已知强酸与强碱在稀溶液里反应的中和热可表示为
H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1对下列反应:
CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-Q1 kJ•mol-1
$\frac{1}{2}$H2SO4(浓)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-Q2 kJ•mol-1
HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l)△H=-Q3 kJ•mol-1
上述反应均在溶液中进行,则下列Q1、Q2、Q3的关系正确的是A
A.Q2>Q3>Q1 B.Q2>Q1>Q3 C.Q1=Q2=Q3 D.Q2=Q3>Q1.
3.目前下列工艺过程没有直接使用离子交换技术的是( )
| A. | 硬水的软化 | B. | 电解饱和食盐水制造NaOH | ||
| C. | 电渗析淡化海水 | D. | 海水中提取金属Mg |
7.同温同压下,xg的甲气体和Yg的乙气体占有相同的体积,根据阿伏伽德罗定律判断,下列叙述错误的是( )
| A. | x:y等于等质量的甲和乙的分子个数之比 | |
| B. | x:y等于同温同压下甲和乙的密度之比 | |
| C. | x:y等于甲与乙的相对分子质量之比 | |
| D. | x:y等于同温同体积下等质量的甲和乙的压强之比 |
