题目内容
7.下列离子方程式中,不正确的是( )| A. | 将SO2气体通入三氯化铁溶液中:SO2+2Fe3++2H2O=2Fe2++SO42-+4H+ | |
| B. | 铜和三氯化铁溶液反应:Cu+Fe3+=Fe2++Cu2+ | |
| C. | 实验室制取氯气:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| D. | 金属铝投入到NaOH溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
分析 A.发生氧化还原反应,遵循电子、电荷守恒;
B.电子、电荷不守恒;
C.反应需要加热,生成氯化锰、氯气和水;
D.反应生成偏铝酸钠和氢气.
解答 解:A.将SO2气体通入三氯化铁溶液中的离子反应为SO2+2Fe3++2H2O=2Fe2++SO42-+4H+,故A正确;
B.铜和三氯化铁溶液反应的离子反应为Cu+2Fe3+=2Fe2++Cu2+,故B错误;
C.实验室制取氯气的离子反应为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,故C正确;
D.属铝投入到NaOH溶液中的离子反应为2Al+2OH-+2H2O=2AlO2-+3H2↑,故D正确;
故选B.
点评 本题考查离子反应的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应的离子反应及分析与应用能力的考查,题目难度不大.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
17.化学与生活息息相关,下列说法错误的是( )
| A. | 用SO2漂白过的草帽辫日久会变色 | |
| B. | 硅胶多孔,常用作食品干燥剂和催化剂的载体 | |
| C. | 用灼烧和闻气味的方法区别棉织物和纯毛织物 | |
| D. | 氯气处理饮用水,在夏季的杀菌效果比在冬季好 |
18.NA表示阿伏伽德罗常数.下列叙述中正确的是( )
| A. | 标准状况下,22.4 L水中含有的水分子数为NA | |
| B. | 4.0 g NaOH固体溶于100 mL水中,得到1 mol/L的 NaOH溶液 | |
| C. | 常温、常压下,22 g CO2中含有的氧原子数为NA | |
| D. | 0.5 mol/L Na2SO4溶液中,含有的离子总数为1.5NA |
15.下列说法正确的是( )
| A. | 高纯硅广泛用于制作光导纤维 | |
| B. | 将SO2通入到BaCl2溶液中可生成白色沉淀 | |
| C. | 向AlCl3溶液中滴加氨水,产生白色沉淀,再加过量的NaHSO4溶液,沉淀消失 | |
| D. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
19.下列不含有共价键的化合物是( )
| A. | CaCl2 | B. | NaOH | C. | NH4Cl | D. | H2O |
16.常温下,有关下列溶液叙述正确的是( )
| A. | 某醋酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则b=a+1 | |
| B. | 某溶液由水电离的c(OH-)=1.0x10-13mol/L,则此溶液一定显酸性 | |
| C. | 将pH=4的醋酸稀释1000倍,溶液的pH=7 | |
| D. | pH=13的强碱溶液和pH=2的强酸溶液混合,若所得溶液的pH=7,则强碱与强酸的体积比是1:10 |
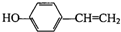 ,其含氧官能团的名称为羟基;
,其含氧官能团的名称为羟基;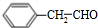 ;
;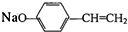 +H2O
+H2O