题目内容
下列事实不能用勒夏特列原理解释的是( )
| A、升高温度能够增大0.1mol?L-1的HF的电离程度 |
| B、合成NH3反应中,为提高NH3的产率,理论上应采取相对较低温度的措施 |
| C、对平衡体系:CO(g)+NO2(g)?CO2(g)+NO(g)加压,可使颜色变深 |
| D、溴水中存在平衡:Br2+H2O?HBr+HBrO,加入AgNO3溶液后,溶液颜色变浅 |
考点:化学平衡移动原理
专题:化学平衡专题
分析:勒沙特列原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动.勒沙特列原理适用的对象应存在可逆过程,如与可逆过程无关,则不能用勒沙特列原理解释.
解答:
解:A.HF为弱电解质,电离吸热,加热促进电离,可用勒夏特列原理解释,故A不选;
B.合成氨反应为放热反应,降低温度平衡正向移动,增大氨气的产率,可用勒夏特列原理解释,但实际生产时还要考虑反应速率以及催化剂的活性,故B不选;
C.增大压强,平衡不移动,但浓度增大,颜色加深,与能用勒夏特列原理解释,故C选;
D.加入AgNO3溶液后,生产AgBr沉淀,平衡正向移动,溴水浓度降低,颜色变浅,可用勒夏特列原理解释,故D不选.
故选C.
B.合成氨反应为放热反应,降低温度平衡正向移动,增大氨气的产率,可用勒夏特列原理解释,但实际生产时还要考虑反应速率以及催化剂的活性,故B不选;
C.增大压强,平衡不移动,但浓度增大,颜色加深,与能用勒夏特列原理解释,故C选;
D.加入AgNO3溶液后,生产AgBr沉淀,平衡正向移动,溴水浓度降低,颜色变浅,可用勒夏特列原理解释,故D不选.
故选C.
点评:本题考查了勒夏特列原理的使用条件,为高频考点,题目难度不大,注意使用勒夏特列原理的前提必须是可逆过程.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、16g O3与 O2混合物中所含氧原子数为NA |
| B、2.3gNa+中含有的电子数为0.1NA |
| C、在常温常压下11.2L二氧化碳所含的分子数目为0.5NA |
| D、相同质量的两块钠分别变成氧化钠和过氧化钠前者失去的电子数多 |
下列离子方程式书写正确的是( )
| A、铁与盐酸反应:Fe+2H+=Fe3++H2↑ |
| B、氢氧化钡溶液和稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| C、氯化铝中加入过量的氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| D、向水玻璃中加盐酸:SiO32-+2H+=H2SiO3↓ |
绿色植物是空气天然的净化器,1万平方米柳杉每月可以吸收160kg SO2,则1万平方米柳杉每月吸收的SO2的物质的量为( )
| A、164 kg |
| B、2.5 mol |
| C、2 500 mol |
| D、2 500 g/mol |
把7.2g铁粉投入40ml某HNO3溶液中,充分反应后剩余固体1.6g,产生NO2和NO的混合气体0.08mol.若不考虑N2O4的存在,则原HNO3溶液的物质的量浓度( )
| A、3.5 mol?l -1 |
| B、4.5 mol?l -1 |
| C、7.0 mol?l -1 |
| D、9.0 mol?l -1 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
①将1mol氯气通入一定量水中发生反应转移电子数为NA
②12.0g熔融的NaHSO4中含有的阳离子数为0.1NA
③在标准状况下,22.4L辛烷中的分子数为NA
④1mol羟基中含有的电子数为10NA
⑤1mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA.
①将1mol氯气通入一定量水中发生反应转移电子数为NA
②12.0g熔融的NaHSO4中含有的阳离子数为0.1NA
③在标准状况下,22.4L辛烷中的分子数为NA
④1mol羟基中含有的电子数为10NA
⑤1mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA.
| A、②⑤ | B、④⑤ |
| C、①③⑤ | D、③④⑤ |
甲、乙、丙、丁均为中中学化学常见物质,一定条件下它们有如下转化关系(其他产物已略去),下列说法正确的是( )


| A、若丁为KOH溶液,则甲可能为Al |
| B、若丁为Fe,则丙可能为Fe(NO3)2溶液 |
| C、若丁为O2,则甲可为非金属单质硫 |
| D、若甲、乙、丙均为焰色反应呈黄色的化合物,则丁一定为CO2 |
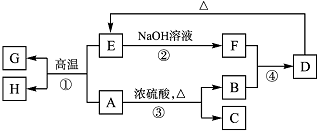 已知A、B、C、D、E、F、G、H可以发生如下图所示的转化(反应过程中部分产物已略去).其中,A、G为同一主族元素的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物.
已知A、B、C、D、E、F、G、H可以发生如下图所示的转化(反应过程中部分产物已略去).其中,A、G为同一主族元素的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物.