题目内容
【题目】铜和铜合金广泛用于电气、机械制造、建筑工业、国防工业等领域。
(1)以含Cu2S80%的精辉铜矿为原料冶炼金属铜(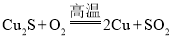 )。若生产含Cu量为97.5%的粗铜48t,则生产SO2_________L(标准状况下);需要精辉铜矿_______t(保留一位小数)。
)。若生产含Cu量为97.5%的粗铜48t,则生产SO2_________L(标准状况下);需要精辉铜矿_______t(保留一位小数)。
(2)高温时,Cu2S和O2在密闭容器中实际发生的反应为以下两步:
2Cu2S+3O2![]() 2Cu2O+ 2SO2、2Cu2O+ Cu2S
2Cu2O+ 2SO2、2Cu2O+ Cu2S![]() 6Cu+ SO2↑
6Cu+ SO2↑
取amol Cu2S和bmol空气(设氧气占空气体积的20%)在高温下充分反应。根据下列几种情况回答问题(反应前后温度、容器体积不变):
①若反应后剩余固体只有Cu,则a和b的关系是___________。
②若反应后剩余固体是Cu2S和Cu,则反应前容器内压强(P1)与反应后容器内压强(P2)的关系是_______。
③若反应后容器内的压强小于反应前,通过分析,确定反应前后容器内固体的成分___________。
(3)可用纯度为80%的精辉铜矿制备胆矾。称取8.0g矿样,溶解在40mL14.0mol/L的浓硝酸中(杂质不反应),反应为: 2Cu2S+14H++10NO3-→4Cu2++2SO42-+5NO↑+5NO2↑+7H2O。过滤后向所得溶液再加入适量的铜和稀硫酸,充分反应前后,将该溶液蒸发结晶。计算理论上最多可得到CuSO4·5H2O晶体多少克_______?
【答案】8.19×106 L 73.1t b=5a P1=P2 Cu2O、Cu和Cu2O 155
【解析】
(1)设日均产SO2标准状况下体积为y,根据元素守恒:

所以48×97.5%×106:![]() =128:1
=128:1
解得y=8.19×106
设需精辉铜矿的质量为x,根据元素守恒:

所以x80%:48×97.5%×106=160:128
解得x=73.1×106=73.1t
(2)①反应后固体全部是Cu时,则:2Cu2S+3O2![]() 2Cu2O+2SO2、2Cu2O+Cu2S
2Cu2O+2SO2、2Cu2O+Cu2S![]() 6Cu+ SO2↑,两方程式相加得:
6Cu+ SO2↑,两方程式相加得:

解得b=5a
故答案为:b=5a;
②Cu2S+O2=2Cu+SO2,反应后固体为Cu2S、Cu时,氧气不足,但反应前后气体的体积未变,所以P1=P2,
故答案为:P1=P2;
③2Cu2S+3O2=2Cu2O+2SO2,消耗3mol氧气生成2mol二氧化硫,当产物为Cu2O时,反应后容器内的压强小于反应前,Cu2S+O2=2Cu+SO2,反应后固体为Cu时,反应前后气体的体积未变,P1=P2,但反应后固体为Cu2O、Cu时,反应后容器内的压强小于反应前,所以反应后容器内的压强小于反应前,反应前为Cu2S,反应后容器内固体的成分为Cu2O或Cu和Cu2O,
故答案为:Cu2O或Cu和Cu2O;
(3)纯度为80%的精辉铜矿8.0g矿样,含铜n(Cu)=![]() ×2=0.08mol,可生成n(CuSO45H2O)=0.08mol,矿样溶解在40mL14.0mol/L的浓硝酸中(杂质不反应),2Cu2S+14H++10NO3-=4Cu2++2SO42-+5NO↑+5NO2↑+7H2O消耗硝酸n(HNO3)=
×2=0.08mol,可生成n(CuSO45H2O)=0.08mol,矿样溶解在40mL14.0mol/L的浓硝酸中(杂质不反应),2Cu2S+14H++10NO3-=4Cu2++2SO42-+5NO↑+5NO2↑+7H2O消耗硝酸n(HNO3)=![]() ×
×![]()
=0.2mol,过滤后向所得溶液再加入适量的铜和稀硫酸,相当于铜溶解在稀硝酸中,然后全部转化为硫酸铜晶体,n(HNO3)=(0.56-0.2)mol=0.36mol,2NO3-+3Cu+8H+=3Cu2++2NO↑+4H2O,溶解铜n(Cu)=![]() ×3=0.54mol,则消耗的铜的总的物质的量为n(Cu)=0.54mol+0.08mol=0.62mol,根据铜原子守恒,理论上最多可得到CuSO45H2O晶体m(CuSO45H2O)=n×M=0.62mol×250g/mol=155g,
×3=0.54mol,则消耗的铜的总的物质的量为n(Cu)=0.54mol+0.08mol=0.62mol,根据铜原子守恒,理论上最多可得到CuSO45H2O晶体m(CuSO45H2O)=n×M=0.62mol×250g/mol=155g,
故答案为:155。

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案【题目】钢铁制品经常进行烤蓝处理,即在铁制品的表面生成一层致密的Fe3O4。某学习小组为了研究烤蓝铁片,分别进行了以下实验操作:
①把一定量烤蓝铁片加工成均匀粉末。
②取m g该粉末,放入28.00 mL 1 mol/L的盐酸中,恰好完全反应,生成标准状况下的气体134.4 mL,向溶液中滴入KSCN溶液,无明显现象。
③再取三份不同质量的粉末,分加加到相同体积(V)、物质的量浓度均为l0.00 mol/L的三份硝酸溶液中,充分反应后,固体全部溶解,有关的实验数据如下表所示(假设NO是硝酸的唯一还原产物):
实验序号 | Ⅰ | Ⅱ | Ⅲ |
加入粉末质量/g | 13.68 | 27.36 | 34.20 |
生成气体的体积(标准状况)/L | 2.912 | 5.824 | 6.720 |
完成下列各题:
(1)实验②所得溶液中的溶质是_______(写化学式),样品中n(Fe)∶n(Fe3O4)=________,m=____________。
(2)计算实验③中每份硝酸溶液的体积(V)(mL)_________。
(3)若向实验Ⅱ所得溶液中继续加入铜粉,要使溶液中Cu2十、Fe2+、Fe3+同时存在,求加入铜粉的物质的量的范围___________。