题目内容
【题目】高铁酸钾(K2FeO4,暗紫色固体),是一种新型、高效、多功能的水处理剂。完成下列填空:
(1)K2FeO4溶于水得到浅紫红色的溶液,且易水解,生成氧气和氢氧化铁。写出该水解反应的离子方程式_________;说明高铁酸钾做水处理剂的原理______。
(2)下图分别是1mol/L的K2FeO4溶液在不同pH和温度下c(FeO42-)随时间的变化曲线。
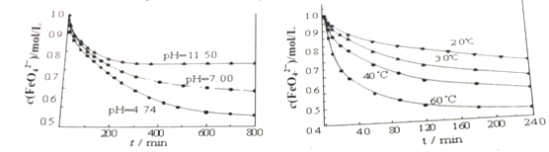
根据以上两图,说明配制K2FeO4溶液的注意事项______________。
【答案】4FeO42-+10H2O![]() 4Fe(OH)3+8OH-+3O2↑ 强氧化性;杀菌消毒 低温、碱性条件下配制溶液
4Fe(OH)3+8OH-+3O2↑ 强氧化性;杀菌消毒 低温、碱性条件下配制溶液
【解析】
(1)用2FeO4处理中性废水时与水反应生成氢氧化铁胶体,并放出无色无味的气体和其它物质,铁元素化合价降低,氧元素化合价升高生成氧气,结合电荷守恒配平书写离子方程式为:4FeO42-+10H2O![]() 4Fe(OH)3+8OH-+3O2↑;高铁酸根离子具有强氧化性,能杀菌消毒,氢氧化铁吸附水中的悬浮物,因此高铁酸钾可做水处理剂;
4Fe(OH)3+8OH-+3O2↑;高铁酸根离子具有强氧化性,能杀菌消毒,氢氧化铁吸附水中的悬浮物,因此高铁酸钾可做水处理剂;
(2)高铁酸根离子水解方程式:4FeO42-+10H2O![]() 4Fe(OH)3+8OH-+3O2↑,依据图中数据可知升高温度,减小pH值,高铁酸根离子浓度降低,所以应在低温、碱性条件下配制高铁酸钾溶液。
4Fe(OH)3+8OH-+3O2↑,依据图中数据可知升高温度,减小pH值,高铁酸根离子浓度降低,所以应在低温、碱性条件下配制高铁酸钾溶液。

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
【题目】用如图所示装置进行下列实验:将①中溶液逐滴滴入②中,预测的现象与实际相符的是
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
|
A. | 稀盐酸 | 浓碳酸钠溶液 | 立即产生气泡 | |
B. | 浓硝酸 | 用砂纸打磨过的铝条 | 产生大量红棕色气体 | |
C. | 氯化亚铁溶液 | 过氧化钠固体 | 产生气体和红褐色沉淀 | |
D. | 氢氧化钠溶液 | 氧化铝粉末 | 产生白色沉淀 |
A.AB.BC.CD.D