题目内容
如图的结构图中,均为由短周期元素的原子构成的分子,●代表原子实(原子实是原子除去最外层电子后剩余部分),小黑点代表未用于形成共价键的最外层电子,一条短线代表一对共用电子对.图甲和图乙所表示的分子依次是( )


| A、HClO、AlCl3 |
| B、NaOH、NH3 |
| C、LiOH、PCl3 |
| D、HCN、BF3 |
考点:原子核外电子排布
专题:
分析:根据原子的成键特点:H原子只能形成一个共价键,C原子能形成4个共价键,N原子形成3个共价键,还有一个孤电子对,B原子形成3个共价键,卤素原子形成1个共价键还有3个孤电子对,据此分析.
解答:
解:常见原子的成键特点:H原子只能形成一个共价键,C原子能形成4个共价键,N原子形成3个共价键,还有一个孤电子对,B原子形成3个共价键,卤素原子形成1个共价键还有3个孤电子对,则甲图中对应化合物为H-C≡N,即HCN,乙图中对应的化合物为BF3;
故选D.
故选D.
点评:本题考查了常见元素的成键特点,题目难度不大,注意把握原子形成的共价键数目与其原子核外的单电子数有关.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
白色污染的危害主要有( )
①破坏土壤结构、降低土壤肥效 ②焚烧产生有毒气体,污染环境 ③释放出氟氯代烷破坏臭氧层 ④危害动物 ⑤加剧温室效应 ⑥引起赤潮.
①破坏土壤结构、降低土壤肥效 ②焚烧产生有毒气体,污染环境 ③释放出氟氯代烷破坏臭氧层 ④危害动物 ⑤加剧温室效应 ⑥引起赤潮.
| A、全部 | B、①②③④⑤ |
| C、③④⑤⑥ | D、①②⑤⑥ |
下列说法正确的是( )
| A、将氯化铝溶液加热,蒸干后得到无水氯化铝固体 |
| B、向Fe(OH)3胶体通电,发现胶体向正极移动,根据电场的作用,我们可以得出,Fe(OH)3带负电 |
| C、23Na37Cl中的质子数和中子数之比7:8 |
| D、硝酸铝溶液中滴加少量的氢氧化钠生成Al(OH)3 |
氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是( )
A、 |
B、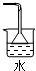 |
C、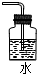 |
D、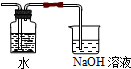 |
已知A物质的分子结构简式如图 ,lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )
,lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )
 ,lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )
,lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )| A、6mol | B、7mol |
| C、9mo1 | D、10mo1 |
配制100mL 1mol/L NaCl溶液,下列操作中错误的是( )
| A、在托盘天平上放两片大小一样的纸,然后将氯化钠放在纸片上称量 |
| B、把称得的氯化钠放入盛有适量蒸馏水的烧杯中,溶解、冷却,再把溶液移入容量瓶中 |
| C、用蒸馏水洗涤烧杯、玻璃棒2~3次,洗涤液也移入容量瓶中 |
| D、沿玻璃棒往容量瓶中加入蒸馏水,直至溶液凹液面恰好与刻度线相切 |
利用红外光谱对有机化合物分子进行测试并记录,可初步判断该有机物分子拥有的( )
| A、同分异构体数 |
| B、原子个数 |
| C、官能团种类 |
| D、分子中的电子数 |
