题目内容
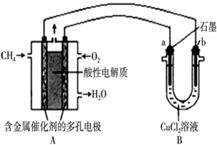 如图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图:
如图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图:请回答:
①甲烷燃料电池的负极反应式为
②当线路中有0.6mol电子通过时,B中阳极产物的质量为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:①甲烷燃料酸性电池中,负极上甲烷失电子和水生成氢离子和二氧化碳;
②b电极为阴极,阴极上铜离子放电生成Cu,根据Cu和转移电子之间的关系式计算.
②b电极为阴极,阴极上铜离子放电生成Cu,根据Cu和转移电子之间的关系式计算.
解答:
解:①甲烷燃料酸性电池中,负极上甲烷失电子和水生成氢离子和二氧化碳,电极反应为CH4-8e─+2H2O=CO2+8H+,故答案为:CH4-8e─+2H2O=CO2+8H+;
②a电极为阳极,阳极上氯离子放电生成氯气,50mL2mol/L的氯化铜溶液含有氯离子是0.2mol,只能转移电子0.2mol,根据氯气和转移电子之间的关系式得析出氯气的质量=0.1mol×71g/mol=7.1g,剩余的电子是在氢氧根失电子生成的氧气过程转移的,转移0.4mol电子会生成氧气0.1mol,质量是3.2g,所以阳极上产物的质量是7.1g+3.2g=10.3g,故答案为:10.3.
②a电极为阳极,阳极上氯离子放电生成氯气,50mL2mol/L的氯化铜溶液含有氯离子是0.2mol,只能转移电子0.2mol,根据氯气和转移电子之间的关系式得析出氯气的质量=0.1mol×71g/mol=7.1g,剩余的电子是在氢氧根失电子生成的氧气过程转移的,转移0.4mol电子会生成氧气0.1mol,质量是3.2g,所以阳极上产物的质量是7.1g+3.2g=10.3g,故答案为:10.3.
点评:本题涉及燃料电池的工作原理以及原电池的工作原理以及计算等知识,注意电子守恒的计算是重点,难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
下列有关说法正确的是( )
| A、金属钠、镁着火时可用泡沫灭火器扑灭 |
| B、为防止试管破裂,加热固体时试管口一般要略高于试管底 |
| C、1L PH=13的Ba(OH)2溶液中含有0.2NA个OH- 离子 |
| D、1.2克CH4所含有的共价键数与0.1 mol NH3所含的共价键数相同 |
用二氧化锰作催化剂分解氯酸钾制得的氧气,往往具有特殊的异味,这种气体通过KI-淀粉溶液时,溶液变蓝.氧气中可能混有( )
| A、Cl2 |
| B、N2 |
| C、Br2 |
| D、F2 |
下列离子方程式正确的是( )
| A、用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+C02↑ |
| B、Fe2(SO4)3和Ba(OH)2溶液混合:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |
| C、硫酸工业尾气中的SO2用过量的氨水吸收:2NH3?H2O+SO2=2NH4++SO32-+H2O |
| D、Cu溶于浓HNO3:Cu+4H++2NO3一=Cu2++2NO↑+4H2O |
化学与科技、社会、生产、生活密切相关.下列有关说法不正确的是( )
| A、物质燃烧时产生有色火焰的都是焰色反应的见证 |
| B、棉花、木材和植物秸秆的主要成分都是纤维素 |
| C、航天服主要成分由碳化硅陶瓷和碳纤维复合而成,是一种复合材料 |
| D、天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源 |
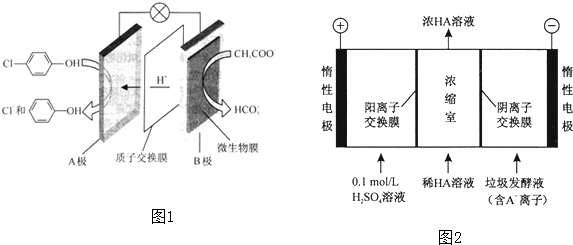
 )的废水可以通过构成微生物电池除去,其原理如图1所示.
)的废水可以通过构成微生物电池除去,其原理如图1所示.