题目内容
同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成还是分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
P4(s,白磷)+5O2(g)====P4O10(s)
ΔH=-2 983.2 kJ·mol-1①
P(s,红磷)+![]() ====
====![]()
ΔH=-738.5 kJ·mol-1②
则白磷转化为红磷的热化学方程式为_________。相同状况下,能量状态较低的是_________;白磷的稳定性比红磷_________(填“高”或“低”)。
P4(s,白磷)====4P(s,红磷)
ΔH=-29.2 kJ·mol-1 红磷 低
解析:
①-4×②得P4(s,白磷)=4P(s,红磷) ΔH=ΔH1-4ΔH2=-2 983.2 kJ·mol-1-4×(-738.5 kJ·mol-1)=-29.2 kJ·mol-1,即P4(s,白磷)====4P(s,红磷) ΔH=-29.2 kJ·mol-1。白磷转化为红磷是放热反应,稳定性比红磷低(能量越低越稳定)。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
(6分)填空:
(1)在测定硫酸铜结晶水含量实验过程中,称量操作至少进行 次。当加热到
时,停止加热,并将坩埚放在 中冷却。当 时则可认为结晶水已经完全失去。实际操作中,有些操作会使实验结果偏高或偏低。下列操作会使测定结果偏高的是 (填字母)
| A.加热温度过高而使硫酸铜部分分解 | B.坩埚用水洗后没有烘干 |
| C.加热后放在空气中冷却 | D.粉末未完全变白就停止加热 |
P(s、红磷)+5/4O2(g)=1/4P4O10(s);△H=-738.5kJ·mol-1
由此可知白磷的稳定性比红磷_____。(填写“强”或“弱”)
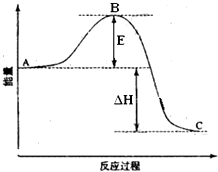 Ⅰ同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算.
Ⅰ同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算.