题目内容
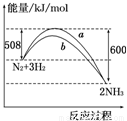
 如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )分析:A、依据热化学方程式的书写原则判断,△H=放出的能量-吸收的能量;
B、根据催化剂与能耗的关系分析;
C、根据升高温度对速率的影响是增大反应速率;
D、反应是可逆反应;
B、根据催化剂与能耗的关系分析;
C、根据升高温度对速率的影响是增大反应速率;
D、反应是可逆反应;
解答:解:A、该反应放出的能量大于吸收的能量,所以放热,书写热化学方程式必须标注物质的聚集状态,该热化学方程式未标注物质的状态,故A错误;
B、催化剂能改变反应的路径,使发生反应所需的活化能降低,即可降低生产能耗,故B正确;
C、升高温度,正逆反应速率都增大,增大程度不同,平衡逆向移动,故C错误;
D、反应是可逆反应,在温度、体积一定的条件下,通入1 mol N2和3 mol H2充分反应后放出的热量小于92 kJ,故D错误;
故选B.
B、催化剂能改变反应的路径,使发生反应所需的活化能降低,即可降低生产能耗,故B正确;
C、升高温度,正逆反应速率都增大,增大程度不同,平衡逆向移动,故C错误;
D、反应是可逆反应,在温度、体积一定的条件下,通入1 mol N2和3 mol H2充分反应后放出的热量小于92 kJ,故D错误;
故选B.
点评:本题考查了热化学方程式的书写方法和要求,图象分析能力,主要是催化剂的概念,对反应影响的实质和结果.

练习册系列答案
相关题目
 (2012?吉林一模)实验发现,298K时,在FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+.某化学兴趣小组根据该实验事实设计了如图所示的原电池装置.下列有关说法中正确的是( )
(2012?吉林一模)实验发现,298K时,在FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+.某化学兴趣小组根据该实验事实设计了如图所示的原电池装置.下列有关说法中正确的是( )