题目内容
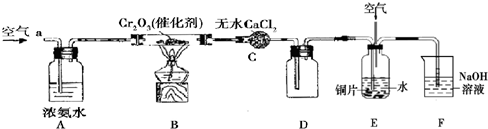
按下图装置进行实验,并回答下列问题
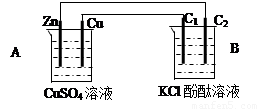
⑴判断装置的名称:A池为___________ B池为______________
⑵锌极为__________极,电极反应式为_________________________
石墨棒C2附近发生的实验现象为_______________________________
⑶当C2极析出224mL气体(标准状态)时,锌的质量变化_________(变大、不变或变小)了_________g。
【答案】
⑴原电池;电解池 ⑵ 负极 ;Zn-2e—=Zn2+;有气泡放出,溶液变红⑶ 变小 ;0.65g
【解析】
试题分析:(1)锌和硫酸铜的反应是自发进行的,所以A是原电池,B电解池。
(2)锌比铜活泼,锌是负极失去电子,电极反应式是Zn-2e—=Zn2+;石墨棒C2与锌电极相连,则是阴极,溶液中的氢离子放电生成氢气,所以发生的实验现象为有气泡放出,溶液变红。
(3)当C2极析出224mL气体(标准状态)时,即氢气的物质的量是0.01mol,反应中转移0.02mol电子,则根据电子的得失守恒可知锌的质量减少0.65g。
考点:考查原电池、电解池的判断,电极名称的判断阴极电极反应式的书写和有关计算
点评:该题是高考中的常见题型,属于基础性试题的考查,难度不大。主要是考查学生对电化学工作原理的熟悉掌握程度,侧重对学生基础性知识的考查和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
 某课外活动小组对甲酸进行了如下的实验,以验证其含有醛基,并考察其化学性质.首先做了银镜反应:
某课外活动小组对甲酸进行了如下的实验,以验证其含有醛基,并考察其化学性质.首先做了银镜反应: 和CH3CH2-18OH进行酯化反应的化学方程式
和CH3CH2-18OH进行酯化反应的化学方程式