题目内容
下列各组热化学方程式中ΔH1小于ΔH2的是
(1)S(s)+O2(g)===SO2(g),ΔH1
S(g)+O2(g)===SO2(g),ΔH2
(2)CH4(g)+2O2(g)===CO2(g)+2H2O(l),ΔH1
CH4(g)+1.5O2(g)===CO(g)+2H2O(g),ΔH2
(3)4Al(s)+3O2(g)===2Al2O3(s),ΔH1
4Fe(s)+3O2(g)===2Fe2O3(s),ΔH2
(4)放热反应CO(g)+2H2(g) CH3OH(g)ΔH1
CH3OH(g)ΔH1
CO(g)+2H2(g) CH3OH(l)ΔH2
CH3OH(l)ΔH2
A.只有(2) B.只有(2 ) (4)
C.只有(1) (2 ) (4) D.只有(2 ) (3)
| A. | 质量不等、密度相等的N2和C2H4 | B. | 等体积等密度的CO和N2 | ||
| C. | 等温等体积的O2和N2 | D. | 等压等体积的N2和CO2 |
完成下列表格(注明单位):
微粒 | 摩尔质量 | 质量 | 物质的量 | 微粒数 |
O | 16g/mol | 16g | ||
N2 | 0.5mol | |||
Cu | 64g/mol | 2NA | ||
H2SO4 | 1.5NA |
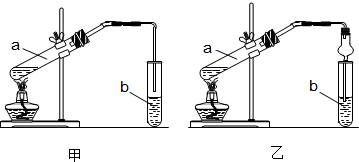
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡,混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案:
编号[ | H | 酸性KMnO4溶液 | 温度/℃ | ||
浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.01 | 4.0 | 50 |

(1)该反应的离子方程式为____________________________;
(2)探究温度对化学反应速率影响的实验编号是 ,探究反应物浓度对化 学反应速率影响的实验编号是 ;
学反应速率影响的实验编号是 ;
(3)实验①测得K MnO4溶液的褪色时间为40 s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)= mol·L-1·min-1;
MnO4溶液的褪色时间为40 s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)= mol·L-1·min-1;
(4)该反应的速率v和时间t的关系如图所示,在t1~t2时段反应速率________(填“加快”或“减慢”或“变化不明显”),主要原因是_____________________。


 2C2O4溶液[
2C2O4溶液[ Z(g)+W(s);△H>0,下列叙述正确的是
Z(g)+W(s);△H>0,下列叙述正确的是 H2(g)+Br2(g),下列四个图中可以表示该反应在一定条件下为可逆反应的是
H2(g)+Br2(g),下列四个图中可以表示该反应在一定条件下为可逆反应的是 B.
B. C.
C. D.
D.