题目内容
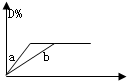 已知反应3A(g)+2B(g)?C(g)+4D(g);△H<0.如图:a、b表示在一定条件下,D的体积分数D%随时间t的变化情况.若使曲线b变为曲线a,可采取的措施是①增加C的质量 ②升高温度 ③缩小反应容器的容积(加压)④减小B的浓度 ⑤使用适当催化剂( )
已知反应3A(g)+2B(g)?C(g)+4D(g);△H<0.如图:a、b表示在一定条件下,D的体积分数D%随时间t的变化情况.若使曲线b变为曲线a,可采取的措施是①增加C的质量 ②升高温度 ③缩小反应容器的容积(加压)④减小B的浓度 ⑤使用适当催化剂( )| A、只有⑤ | B、①③ |
| C、③⑤ | D、②③⑤ |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:使b曲线变为a曲线,到达平衡时间缩短,且D的体积发生不变,说明改变条件,反应速率加快,不影响平衡移动,据此结合选项解答.
解答:
解:①C是固体,增加C的质量,平衡不移动,不能加快反应速率,故①错误;
②升高温度,反应速率加快,该反应正反应是放热反应,升高温度,平衡向逆反应移动,D的体积分数降低,故②错误;
③缩小反应容器的体积增大压强,反应速率加快,该反应前后气体的物质的量不变,平衡不移动,D体积分数不变,故③正确;
④减小B的浓度,反应速率降低,平衡向逆反应进行,D的体积分数降低,故④错误;
⑤使用适当催化剂缩短反应达到平衡时间,平衡不动,D的体积分数降低,故⑤正确;
故选C.
②升高温度,反应速率加快,该反应正反应是放热反应,升高温度,平衡向逆反应移动,D的体积分数降低,故②错误;
③缩小反应容器的体积增大压强,反应速率加快,该反应前后气体的物质的量不变,平衡不移动,D体积分数不变,故③正确;
④减小B的浓度,反应速率降低,平衡向逆反应进行,D的体积分数降低,故④错误;
⑤使用适当催化剂缩短反应达到平衡时间,平衡不动,D的体积分数降低,故⑤正确;
故选C.
点评:本题考查平衡图象、化学平衡的影响因素等,难度中等,关键是根据图象判断改变条件,反应速率加快,不影响平衡移动,明确影响化学平衡的移动因素.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在一固定容积的密闭容器中,加入xmolA和ymolB,发生反应:mA(g)+nB(g)?pC(g),且m+n≠p,则反应处于平衡状态的标志是( )
| A、c(A)=c(B)=c(C) |
| B、单位时间内消耗m mol A,同时消耗n mol B |
| C、单位时内消耗n mol A,同时生成n mol B |
| D、当温度一定时,容器内压强不随时间变化 |
把铁钉和碳棒用导线连接起来后浸入食盐溶液中,可能出现的现象是( )
| A、铁钉上放出氢气 |
| B、铁钉锈蚀 |
| C、碳棒上放出氯气 |
| D、碳棒上放出氧气 |
下列分子或离子中都存在着配位键的是( )
①NH3 ②CH4 ③H3O+ ④CH3COO- ⑤[B(OH)4]-.
①NH3 ②CH4 ③H3O+ ④CH3COO- ⑤[B(OH)4]-.
| A、①② | B、③④ | C、①④ | D、③⑤ |
清洗沾有某些物质的试管,下列方法中不正确的是( )
| A、用酒精清洗沾有碘的试管 |
| B、用稀硝酸清洗沾有银镜的试管 |
| C、用水清洗沾有固体石蜡的试管 |
| D、用乙醇清洗沾有苯酚的试管 |
已知I-、Fe2+、SO2、Cl-、H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Cl-<Fe2+<H2O2<I-<SO2.则下列反应不能发生的是( )
| A、2Fe3++SO2+2H2O=2Fe2++SO2-4+4H+ |
| B、Cl2+SO2+2H2O═H2SO4+2HCl |
| C、H2O2+2H++SO2-4═SO2↑+O2↑+2H2O |
| D、2I2+H2O2=2H2O+O2↑+4I- |
下列说法正确的是( )
| A、18g H2O在标准状况下的体积是22.4L |
| B、22.4L O2中一定含有6.02×1023个氧分子 |
| C、在标准状况时,20mLNH3与60mL N2所含的分子个数为1:3 |
| D、将80g NaOH溶于1L水中,所得溶液中 NaOH的物质的量浓度为2moL/L |
元素X、Y、Z原子序数之和为33,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构.下列推测不正确的是( )
| A、在短周期元素中X的金属性最强 |
| B、原子半径Z>Y,离子半径Z2->X+ |
| C、Y、Z都可与氢元素形成氢化物,Z的氢化物比Y的氢化物稳定性高 |
| D、Y的最高价含氧酸属于弱酸 |
下列表述正确的是( )
| A、人造刚玉熔点很高,可用作高级耐火材料,主要成分是SiO2 |
| B、化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是Al2O3 |
| C、提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料 |
| D、用于现代通讯的光导纤维的主要成分是高纯度的硅 |