题目内容
14.孔雀石呈绿色,是一种名贵的宝石.其主要成分是xCu(OH)2•yCuCO3.某兴趣小组为探究孔雀石组成,利用如图所示的装置(夹持仪器省略)进行实验:
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于硬直玻璃管中.
步骤2:称量相关装置的质量,打开活塞K,鼓入空气,一段时间后关闭.
步骤3:加热装置B直至装置C中无气泡产生.
步骤4:打开K1,继续通一段时间空气至装置冷却 (请补充该步操作内容).

步骤5:冷却至室温,称量相关装置的质量.
(1)孔雀石热分解的化学方程式xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑.
(2)装置A的作用是除去空气中的CO2和H2O;若无装置E,则实验测定的x/y的值将偏小.(选填“偏大”、“偏小”或“无影响”).
(3)某同学在实验过程中采集了如下数据:
A.反应前玻璃管与样品的质量163.8g
B.反应后玻璃管中残留固体质量20g
C.装置C实验后增重2.25g
D.装置D实验后增重5.5g
为测定x/y的值,你认为可以选用上述所采集数据中的BC、BD、CD(写出所有组合的字母代号)任一组即可进行计算,并根据你的计算结果,写出孔雀石组成的化学式Cu(OH)2•CuCO3.
分析 依据实验步骤和目的分析,步骤4是反应完毕后,需要继续通空气,让装置冷却;
(1)xCu(OH)2•yCuCO3加热分解生成氧化铜、二氧化碳气体和水,根据质量守恒定律写出该反应方程式;
(2)根据实验目的和碱石灰的作用分析,装置A碱石灰是干燥剂,可吸收空气中的水分,同时还能吸收空气中的二氧化碳,防止对装置CD增重的数据造成影响,装置E的作用是防止空气中的二氧化碳和水蒸气进入D装置;
(3)根据化学方程式找出与x、y有关的物质质量,对比分析,碱式碳酸铜分解的化学方程xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑要测定x/y,可以测定生成的水和二氧化碳的质量,即测定C装置增重的质量和D装置增重的质量或BC、BD装置质量计算判断;根据计算结果写出该样品组成的化学式.
解答 解:步骤4反应完毕后,需要继续通空气,让装置冷却,所以步骤4为:打开K1,继续通一段时间空气至装置冷却,
故答案为:打开K1,继续通一段时间空气至装置冷却;
(1)xCu(OH)2•yCuCO3加热分解的化学方程式为:xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑,
故答案为:xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑;
(2)装置A碱石灰是干燥剂,可吸收空气中的水分,同时还能吸收空气中的二氧化碳,防止对装置CD增重的数据造成影响,装置E的作用是防止空气中的二氧化碳和水蒸气进入D装置,D装置是吸收生成的二氧化碳的,C装置是吸收生成的水的,如果没有装置E,会使D装置质量增重偏大,即生成的二氧化碳质量偏大,则$\frac{x}{y}$的值会偏小
故答案为:除去空气中的CO2和H2O;偏小;
(5)碱式碳酸铜分解的化学方程xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑要测定x/y的值,可以测定生成的水和二氧化碳的质量,即测定C装置增重的质量和D装置增重的质量,故可选CD,
xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑
18x 44y
2.25g 5.5g
则:$\frac{18x}{2.25g}$=$\frac{44y}{5.5g}$,解得:$\frac{x}{y}$=1:1;
若测出反应后玻璃管中样品的质量以及装置C增重的质量,即已知方程式中氧化铜和水的质量关系,可求出$\frac{x}{y}$的值,故可选BC,
xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑
(x+y)×80 18x
20g 2.25g
则:$\frac{(x+y)×80}{20g}$=$\frac{18x}{2.25g}$,解得:$\frac{x}{y}$=1:1;
同样若已知反应后玻璃管中样品的质量以及装置C增重的质量,即已知方程式中氧化铜和二氧化碳的质量关系,可求出$\frac{x}{y}$的值.故可可选BD,
xCu(OH)2•yCuCO3$\frac{\underline{\;\;△\;\;}}{\;}$(x+y)CuO+xH2O+yCO2↑
(x+y)×80 44y
20g 5.5g
则:$\frac{(x+y)×80}{20g}$=$\frac{44y}{5.5g}$,解得:$\frac{x}{y}$=1:1;
根据以上计算结果可知该样品组成的化学式为:Cu(OH)2•CuCO3,
故答案为:BC、BD、CD;Cu(OH)2•CuCO3.
点评 本题考查探究物质组成测量物质含量的方法,题目难度中等,明确浓硫酸增重的质量是生成的水的质量、碱石灰增重的质量是生成的二氧化碳的质量为解答关键,试题侧重考查学生的分析、理解能力及化学计算、化学实验能力.

 计算高手系列答案
计算高手系列答案| A. | 锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去 | |
| B. | 铝盐在水中可产生胶体,可用于自来水的杀菌消毒 | |
| C. | 太阳能热水器、沼气的利用、乙醇汽油都涉及生物质能的利用 | |
| D. | 李比希燃烧法、钠熔法、铜丝燃烧法、纸层析法都是元素定性分析法 |
| A. | 除去CH4中的C2H4杂质选用溴的CCl4溶液 | |
| B. | 油脂、淀粉、纤维素都属于天然高分子化合物 | |
| C. | 甲苯和乙烯都可与酸性高锰酸钾溶液发生化学反应造成酸性高锰酸钾溶液褪色 | |
| D. | 蛋白质溶液加入CuSO4溶液会析出,这一过程属于蛋白质的盐析 |
①霓虹灯发出有色光
②棱镜分光
③激光器产生激光
④石油蒸馏
⑤凸透镜聚光
⑥燃放的焰火在夜空中呈现五彩缤纷的礼花
⑦日光灯通电发光
⑧冷却结晶.
| A. | ①③⑥⑦ | B. | ②④⑤⑧ | C. | ①③⑤⑥⑦ | D. | ①②③⑤⑥⑦ |
| A. | 苯、甲苯、己烯 | B. | 甲苯、己烯、四氯化碳 | ||
| C. | 己烯、汽油、苯 | D. | 苯、甲苯、二甲苯 |

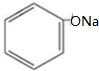 +CO2+H2O→
+CO2+H2O→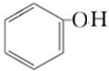 +NaHCO3.
+NaHCO3.