题目内容
4.下列叙述正确的是( )| A. | 过滤时,把待滤液体直接倒入漏斗中 | |
| B. | 蒸发时,待混合物中的水分完全蒸干后,停止加热 | |
| C. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| D. | 向碘水中加入CCl4振荡,有色层在上方 |
分析 A.过滤时,应该用玻璃棒引流;
B.蒸发时,不能蒸干,利用余热加热;
C.分液时,下层液体从下口倒出,上层液体从上口倒出;
D.四氯化碳密度大于水,且碘在四氯化碳中的溶解度大于在水中的溶解度,四氯化碳和水不互溶.
解答 解:A.过滤时,应该用玻璃棒引流,否则易导致滤纸被损坏,故A错误;
B.蒸发时,不能蒸干,利用余热加热,则蒸发时,待混合物中有大量晶体析出时,再停止加热,故B错误;
C.分液时,下层液体从下口倒出,为防止引进杂质,应该将上层液体从上口倒出,故C正确;
D.四氯化碳密度大于水,且碘在四氯化碳中的溶解度大于在水中的溶解度,四氯化碳和水不互溶,所以向碘水中加入CCl4振荡,有色层在下方,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及萃取、分液、蒸发、过滤等知识点,明确实验原理、实验基本操作方法是解本题关键,注意实验操作的规范性和评价性,题目难度不大.

练习册系列答案
相关题目
15.能用酸性高锰酸钾溶液鉴别的一组物质是( )
| A. | 乙烯和乙炔 | B. | 苯和己烷 | C. | 苯和甲苯 | D. | 溴苯和溴乙烷 |
12.六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E同主族,B与F同主族,E与F同周期.已知A与其他元素不在同一周期,D的核电荷数是B的最外层电子数的2倍,单质F是一种重要的半导体材料.则下列推断中正确的是( )
| A. | A、B两种元素可组成化学式为BA2的化合物 | |
| B. | F与D形成的化合物性质很不活泼,不与任何酸反应 | |
| C. | 原子半径由大到小的顺序是E>F | |
| D. | 气态氢化物的稳定性由强到弱的顺序是C>D |
9.下列离子方程式中,正确的是( )
| A. | Al与NaOH溶液的反应:Al3++3OH-=Al (OH) 3↓ | |
| B. | CaCl2溶液与Na2CO3溶液反应:Ca2++CO32-=CaCO3↓ | |
| C. | MgSO4溶液与Ba(OH)2溶液反应:SO42-+Ba2+=BaSO4↓ | |
| D. | CaCO3与稀盐酸反应:CO32-+2 H+=H2CO3 |
16.在由水电离出来的c (H+)=1×10-13mol•L-1溶液中,下列离子可能大量共存的是( )
| A. | NH4+、Ba2+、NO3-、CO32- | B. | Fe2+、Na+、SO42-、MnO4- | ||
| C. | K+、Mg2+、NO3-、SO42- | D. | Na+、Fe3+、Cl-、AlO2- |
13.已知I-、Fe2+、SO2、H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为SO2>I->Fe2+>H2O2,则下列反应不能发生的是( )
| A. | 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ | B. | I2+SO2+2H2O=H2SO4+2HI | ||
| C. | H2O2+H2SO4=SO2+O2+2H2O | D. | 2Fe3++2I-=2Fe2++I2 |
14.配制0.10mol/L乳酸钠(NaC3H5O3)溶液250mL,需用112g/L乳酸钠溶液的体积为( )
| A. | 50mL | B. | 40mL | C. | 25mL | D. | 15mL |
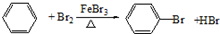 反应类型取代反应.
反应类型取代反应.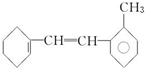 有机物结构简式如下:
有机物结构简式如下: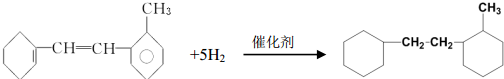 .
.