题目内容
17.氢能是重要的新能源.储氢作为氢能利用的关键技术,是当前关注的热点之一.(1)氢气是清洁燃料,其燃烧产物为水.
(2)NaBH4是一种重要的储氢载体,能与水反应得到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为NaBH4+2H2O=NaBO2+4H2↑,反应消耗1mol NaBH4时转移的电子数目为4mol.
(3)合金储氢是一种新发展起来的储氢技术,利用金属(合金)吸收和释放氢气,循环寿命性能优异,镍氢电池(NiMH)就是采用此技术的电池类型,NiMH中的M表示储氢金属或合金,该电池在放电过程中的总反应方程式是NiOOH+MH═Ni(OH)2+M.
①MH是一类储氢材料,其氢密度越大(填“越大”、“越小”),电池的能量密度越高.
②在放电过程中,正极的电极反应为NiOOH+H2O+e-=Ni(OH)2+OH-,负极的电极反应为MH+OH--e-=M+H2O.
③电池一般使用碱性溶液做电解液(填“酸性溶液”、“碱性溶液”、“中性溶液”).
分析 (1)氢气燃烧的产物只有水;
(2)NaBH4与水反应生成NaBO2,且反应前后B的化合价不变,H元素化合价由-1价、+1价变为0价,结合转移电子守恒配平方程式,判断电子转移数目;
(3)镍氢电池根据总反应:MH+NiOOH=M+Ni(OH)2 ,放电时,正极:NiOOH+H2O+e-=Ni(OH)2+OH-,负极:MH+OH--e-=M+H2O,以上式中M为储氢合金,MH为吸附了氢原子的储氢合金,据此分析解答.
解答 解:(1)依据元素守恒可知,氢气燃烧的产物只有水,故答案为:水;
(2)NaBH4与水发生氧化还原反应生成NaBO2和H2,H元素化合价由-1价、+1价变为0价,要使氧化还原反应得失电子守恒,则反应的化学方程式为:NaBH4+2H2O=NaBO2+4H2↑,依据方程式可知:反应消耗1mol NaBH4时转移的电子数目4mol;
故答案为:NaBH4+2H2O=NaBO2+4H2↑;4mol;
(3)①M为储氢合金,MH为吸附了氢原子的储氢合金,储氢材料,其氢密度越大,电池的能量密度越高;
故答案为:越大;
②镍氢电池根据总反应:MH+NiOOH=M+Ni(OH)2 ,放电时,正极:NiOOH+H2O+e-=Ni(OH)2+OH-,负极:MH+OH--e-=M+H2O,
故答案为:NiOOH+H2O+e-=Ni(OH)2+OH-;MH+OH--e-=M+H2O;
③依据总方程式MH+NiOOH=M+Ni(OH)2 可知:该电池的反应物为碱性物质,应使用碱性溶液做电解质;
故答案为:碱性溶液.
点评 本题考查了氧化还原反应方程式配平及书写,原电池和电解池原理,明确氧化还原反应规律,熟悉原电池、电解池工作原理是解题关键,难点在于电极反应式的书写,题目难度中等.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案
相关题目
5.下列措施中,能减慢化学反应速率的是( )
| A. | 将食物存放在温度低的地方 | |
| B. | 将块状固体药品研细后再反应 | |
| C. | 用MnO2作H2O2分解反应的催化剂 | |
| D. | 用4 mol/LH2SO4溶液代替1 mol/LH2SO4溶液与锌粒反应 |
5.下列说法正确的是( )
| A. | 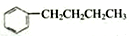 的与H2加成之后的产物中,其一氯代物有7种 的与H2加成之后的产物中,其一氯代物有7种 | |
| B. | CH3CH=CHCH3分子中的四个碳原子在同一直线上 | |
| C. | 按系统命名法,化合物 的名称是2,3,4-三甲基-2-乙基戊烷 的名称是2,3,4-三甲基-2-乙基戊烷 | |
| D. |  的一溴代物和 的一溴代物和  的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) |
2.关于下列各实验装置的叙述中,不正确的是( )


| A. | 图①可用于实验室制备少量Cl2或NH3 | |
| B. | 可用从a处加水的方法检验装置②的气密性 | |
| C. | 实验室也可以用装置③收集HCl气体 | |
| D. | 装置④可用于苯萃取碘水中碘的实验,并把碘的苯溶液从漏斗上口倒出 |
9.下列说法正确的是( )
| A. | 质子数为8、中子数为10的氧原子:${\;}_{8}^{18}$O | |
| B. | 氧原子的结构示意图: | |
| C. | CaCl2的电子式: | |
| D. | 明矾的化学式:KAl(SO4)2 |
6.下列各组的两种物质属于同素异形体的是( )
| A. | ${\;}_{6}^{12}$C和${\;}_{6}^{13}$C | B. | 红磷和白磷 | ||
| C. | 丁烷和异丁烷 | D. | ${\;}_{19}^{40}$K和${\;}_{20}^{40}$Ca |
 在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
在水的电离平衡中,c(H+)和c(OH-)的关系如图所示: