题目内容
6.通常用饱和小苏打溶液除去CO2中的HCl,不能用NaOH溶液,也不能用Na2CO3,不能用Na2CO3的原因是CO32-+CO2+H2O═2HCO3-(用离子方程式表示)分析 碳酸钠能够与二氧化碳、水反应生成碳酸氢钠.
解答 解:碳酸钠能够与二氧化碳、水反应生成碳酸氢钠,离子方程式:CO32-+CO2+H2O═2HCO3-,
故答案为:CO32-+CO2+H2O═2HCO3-.
点评 本题考查了离子方程式的书写,明确发生的化学反应是解答本题的关键,并注意离子反应的书写方法,题目难度不大.

练习册系列答案
相关题目
16.中学化学中很多“规律”都行其使用范围,下列根据有关“规律”推出的结论合理的是( )
| A. | 根据置换反应Na+KCl$\frac{\underline{\;高温\;}}{\;}$NaCl+K↑,推出金属Na的活泼性强于金属K的活泼性 | |
| B. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 | |
| C. | 根据金属活动顺序表推知Sn活泼性强于Pb,推出碱性Sn(OH)4>Pb(OH)4 | |
| D. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
17.在如图所示的原电池中,正极发生的反应是( )


| A. | H2-2e-═2H+ | B. | Cu-2e-═Cu2+ | C. | 2H++2e-═H2↑ | D. | Zn-2e-═Zn2+ |
14.已知反应A+B═C+D为放热反应,对该反应的下列说法正确的是( )
| A. | A的能量一定高于C | |
| B. | A和B的总能量一定低于C和D的总能量 | |
| C. | A和B的总能量一定高于C和D的总能量 | |
| D. | 该反应为放热反应,故不必加热就一定能发生 |
1.下列实验现象描述正确的是( )
| 选项 | 实验 | 现象 |
| A | 加热放在坩埚中的小块钠 | 钠先熔化成光亮的小球,燃烧时火焰为黄色,燃烧后生成淡黄色固体 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化,失去光泽,熔化的铝滴落下来 |
| C | 向久置于空气中的FeSO4溶液中滴加NaOH溶液 | 立刻产生大量白色沉淀 |
| D | 向饱和Na2CO3溶液中通入足量的CO2气体 | 无明显现象 |
| A. | A | B. | B | C. | C | D. | D |
18.a、b、c、d、e都是短周期元素,它们的有关信息如表所示:
(1)上述C元素(填名称)参与形成的物质种类最多.
(2)“神舟九号”飞船内需要有一种由上表中的Na和O元素(填元素符号)组成的化合物来吸收宇航员呼出的CO2.在飞船中为模拟地球上的生态环境,会在太空舱中充入一种气体以稀释O2,这种气体分子的电子式为 .
.
(3)c与e可形成一种化合物,该化合物是光导纤维的主要成分.则该化合物中化学键的类型为共价键(或极性共价键);该物质可溶于d形成的最高价氧化物的水化物,反应的化学方程式为SiO2+2NaOH═Na2SiO3+H2O.
(4)a、b、c、e的最简单氢化物中最稳定的是H2O.
| a | 该元素能形成多种单质,其中一种是自然界中硬度最大的物质 |
| b | 其单质是空气中的主要成分,不能支持燃烧 |
| c | 最外层电子数是次外层电子数的3倍 |
| d | 短周期中最活泼的金属 |
| e | 与a是同主族元素 |
(2)“神舟九号”飞船内需要有一种由上表中的Na和O元素(填元素符号)组成的化合物来吸收宇航员呼出的CO2.在飞船中为模拟地球上的生态环境,会在太空舱中充入一种气体以稀释O2,这种气体分子的电子式为
 .
.(3)c与e可形成一种化合物,该化合物是光导纤维的主要成分.则该化合物中化学键的类型为共价键(或极性共价键);该物质可溶于d形成的最高价氧化物的水化物,反应的化学方程式为SiO2+2NaOH═Na2SiO3+H2O.
(4)a、b、c、e的最简单氢化物中最稳定的是H2O.
16.欲将氯化钠、沙子(主要成分为SiO2)、碘三种物质组成的固体混合物分离,最科学的操作顺序是( )
| A. | 溶解、过滤、加热(升华)、蒸发(结晶) | B. | 加热(升华)、溶解、过滤、蒸发(结晶) | ||
| C. | 加热(升华)、溶解、蒸馏、结晶 | D. | 溶解、结晶、过滤、加热(升华) |

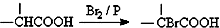
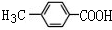 .
.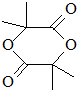 .
.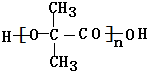 +(n-1)H2O,该反应属于缩聚反应(填反应类型).
+(n-1)H2O,该反应属于缩聚反应(填反应类型).