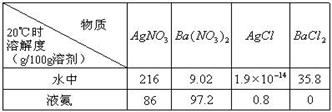
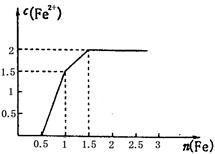
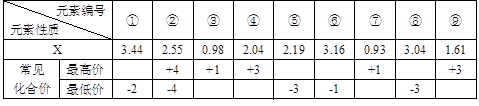��Ŀ����
�������⣨H2O2��O�Ļ��ϼ�Ϊ��1�ۣ��׳�˫��ˮ��ҽ������������ɱ��������������ϴ�˿ڡ��о������漰H2O2�ķ�Ӧ��������и��⣺
A��Ag2O+ H2O2��2Ag+O2 ��+ H2O
B��3H2O2+Cr2(SO4)3+10KOH��2K2CrO4+3K2SO4+8H2O
��1��д��һ��H2O2�����������������ֻ�ԭ�ԵĻ�ѧ��Ӧ����ʽ ��
��2�����������ʣ�H2O2��K2SO4��MnSO4��H2SO4��KMnO4��O2�Ļ�ѧʽ�ֱ����ڿհ״����һ��������ƽ�Ļ�ѧ����ʽ�� + +______ �� + + + H2O
�ٸ÷�Ӧ�еĻ�ԭ���� ��
�ڸ÷�Ӧ�У�������ԭ��Ӧ��Ԫ���� ��
��3�������ԣ�KMnO4_____K2CrO4���������������
��1��2H2O2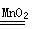 2H2O + O2�� ��2��H2O2+KMnO4+H2SO4��MnSO4+O2+K2SO4+ H2O
2H2O + O2�� ��2��H2O2+KMnO4+H2SO4��MnSO4+O2+K2SO4+ H2O
��H2O2 ��Mn ��3����
���������������1��H2O2�����������������ֻ�ԭ�ԣ���˵���÷�Ӧһ����˫��ˮ�ķֽⷴӦ����Ӧ�Ļ�ѧ����ʽΪ2H2O2 2H2O + O2����
2H2O + O2����
��2��������ؾ���ǿ�����ԣ���������ǿ��˫��ˮ�ģ����Ը�������ܰ�˫��ˮ����������������������صĻ�ԭ�����������̣���˸÷�Ӧ�ķ���ʽ���Ա�ʾΪH2O2+KMnO4+H2SO4��MnSO4+O2+K2SO4+ H2O��
��˫��ˮ����Ԫ�صĻ��ϼ۴ӣ�1�����ߵ�0�ۣ������������˫��ˮ�ǻ�ԭ����
�ڸ��������MnԪ�صĻ��ϼ۴ӣ�7�۽��͵���2�ۣ��õ����ӣ�����ԭ�����Ա���ԭ��Ԫ����Mn��
��3���ڷ�Ӧ3H2O2+Cr2(SO4)3+10KOH��2K2CrO4+3K2SO4+8H2O�У�˫��ˮ����������K2CrO4����������������������������ǿ����������Ŀ�֪����������˫��ˮǿ��K2CrO4���ڷ�ӦH2O2+KMnO4+H2SO4��MnSO4+O2+K2SO4+ H2O�У��������������������������ǿ��˫��ˮ�ģ����Ը�����ص�������ǿ��K2CrO4��
���㣺����������ԭ��Ӧ��Ӧ�á��ж�

 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д���1����ͼ�ǿα��С����ֻ�����Ӧ������������ԭ��Ӧ�Ĺ�ϵ��ͼ����H2+CuO  Cu+H2O����Ӧ����ͼ�е����� ������ţ������з�Ӧ����������7���� ��
Cu+H2O����Ӧ����ͼ�е����� ������ţ������з�Ӧ����������7���� ��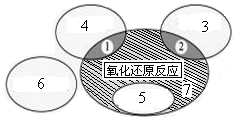
A��2H2+O2 2H2O 2H2O |
B��2NaHCO3 Na2CO3+H2O+CO2�� Na2CO3+H2O+CO2�� |
| C��Zn+H2SO4=ZnSO4+H2�� |
D��CuO+CO Cu+CO2 Cu+CO2 |
O2��H2CrO4��Cr(OH)3��H2O��H2O2
��֪���÷�Ӧ��H2O2ֻ�������¹��̣�H2O2��O2��
�ٸ÷�Ӧ�У�������ԭ��Ӧ�������� ��
��д���÷�Ӧ�Ļ�ѧ����ʽ��������ƽ��
_________+________ �� ________+________+________
��3��3Cl2+8NH3
 N2+6NH4Cl
N2+6NH4Cl����˫�߷���ʾ�÷�Ӧת�Ƶĵ�����Ŀ�ͷ���
�ڸ÷�Ӧ�У��������뻹ԭ�����Ӹ���֮��Ϊ ��
��4����һ�������£�PbO2��Cr3+��Ӧ��������Cr2O72����Pb2+������1molCr3+��ȫ��Ӧ����PbO2�����ʵ���Ϊ ��
��.±�����±�����ڹ�ҵ������������Ҫ�����á�ijС��Ϊ̽������һЩ�ε���
�ʣ��������ϲ�����ʵ�顣�����������£�
�� BrO3�� + 6I�� + 6H+ = 3I2 + Br��+ 3H2O �� 2BrO3�� + I2 = 2IO3�� + Br2
�� IO3�� + 5I�� + 6H+ = 3I2 + 3H2O �� 2IO3�� + 10Br��+ 12H+ = I2 + 5Br2 + 6H2O
ʵ�����£�
| ���� | ���� |
| ��.��ʢ��30 mL 0.2 mol��L-1 KI��Һ����ƿ�����ε��뼸�ε�����Һ������ϡ���ᣬ���õζ�����μ���KBrO3��Һ | ����KBrO3��Һ���룬��Һ����ɫ��Ϊ��ɫ������,���ձ��ֲ��� |
| ��.������������Һ�е���KBrO3��Һ | ��Һ����ɫ����ȥ |
��ش�
��1�����������еķ�Ӧ��~�ܲ������ѧ֪ʶ���ж�IO3����BrO3����I2��Br2����������ǿ������˳���� ��KBrO3��Һ��KBr��Һ�����������·�Ӧ�����ӷ���ʽ�� ��
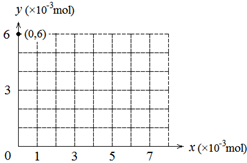
��2������y��ʾ��ƿ�к������ʵ����ʵ��� ����x��ʾ������KBrO3�����ʵ���������ͼ�л�����������ʵ�������y��x�ı仯���ߣ�Ҫ����ͼ�б���յ����꣩��
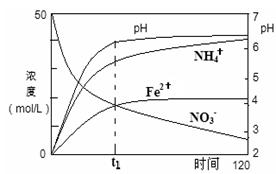
��.��̼�����к��������������ƣ��ס�����λͬѧ����ȡһ�������ĸ���Ʒ����������ͼ��ʾ�����ⶨ��Ʒ�Ĵ��ȡ�����������˳��
��ͬѧ���ݡ��ࡪ�ۡ��ߡ��ܣ� ��ͬѧ���ݡ��ۡ��ڡ�

��֪����̼���ƣ�Na2CO4�����������Ʒֱ������ϡ���ᷴӦ�Ļ�ѧ����ʽ���£�
2Na2CO4��2H2SO4=2Na2SO4��2CO2����O2����2H2O;
2Na2O2��2H2SO4=2Na2SO4��O2����2H2O��
��1����ͬѧ��ͨ��ʵ���õ�������____________����ѡ�õ�װ��________������ţ���û�б�Ҫ�ġ�
��2����ͬѧ��ͨ��ʵ���õ�������________________��������Ϊ������õ����ݼ������ʵ��������ƫ�ߣ�ԭ����________________�� Ϊ�˲��ȷ��ʵ�����ݣ����㽫��ͬѧ��ʵ����ƽ��иĽ���д������ѡ������������˳��ÿ���������ʹ��һ�Σ�Ҳ���Բ��ã���________________������ţ���



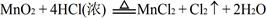 ��������Ϸ�Ӧԭ������MnO2��KMnO4��Cl2����������ǿ������˳���ǣ� ��
��������Ϸ�Ӧԭ������MnO2��KMnO4��Cl2����������ǿ������˳���ǣ� ��