题目内容
1.化学与生活密切相关,下列说法正确的是( )| A. | 碳酸钡可用作“钡餐”,是因为碳酸钡不溶于水 | |
| B. | 雷雨发庄稼是因为雷雨过后空气变得清新 | |
| C. | 聚氯乙烯在食品工业中常用作食品包装袋 | |
| D. | 纯碱可用作锅炉除垢时沉淀硫酸钙的转化剂 |
分析 A.碳酸钡能溶于盐酸,生成可溶性氯化钡;
B.氮气与氧气在放电条件下生成一氧化氮,一氧化氮氧化生成二氧化氮,二氧化氮与水反应生成硝酸,硝酸与盐反应生成可被植物吸收的离子;
C.聚氯乙烯受热分解生成有毒物质;
D.碳酸钙的溶解度小于硫酸钙,依据沉淀转化原则解答.
解答 解:A.碳酸钡能溶于盐酸,生成可溶性氯化钡,钡离子为重金属离子能够引起人体中毒,所以碳酸钡不可用作“钡餐”,故A错误;
B.雷雨天,发生放电现象,氮气与氧气在放电条件下生成一氧化氮,一氧化氮氧化生成二氧化氮,二氧化氮与水反应生成硝酸,硝酸与盐反应生成可被植物吸收的离子,所以雷雨发庄家,故B错误;
C.聚氯乙烯受热分解生成有毒物质,所以聚氯乙烯不能在食品工业中用作包装袋,故C错误;
D.纯碱用作锅炉除垢时CaSO4沉淀的转化剂是因为碳酸钙的溶解度小于硫酸钙,故D正确;
故选:D.
点评 本题考查了物质的性质与用途之间的联系,熟悉物质的性质是解题关键,注意沉淀转化的规律,题目难度中等.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案
相关题目
11.下列说法不正确的是( )
| A. | 浙大研制的石墨烯弹性气凝胶(又名碳海绵)入选2013年度世界最经固体材料,可用作处理海上原油泄漏的吸油材料 | |
| B. | 过氧化氢酶、酚醛树脂、尼龙、有机玻璃、PVC都是高分子化合物 | |
| C. | 生物炼铜的原理是利用某些具有特殊本领的细菌把不溶性的硫化铜转化为铜单质 | |
| D. | 电解熔融氧化铝、粗硅的制取涉及化学变化,煤焦油中提取苯是物理变化 |
12.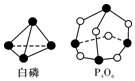 化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和(kJ•mol-1)P-P:198 P-O:360 O=O:498;则反应P4(白磷)+3O2═P4O6的能量变化为( )
化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和(kJ•mol-1)P-P:198 P-O:360 O=O:498;则反应P4(白磷)+3O2═P4O6的能量变化为( )
 化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和(kJ•mol-1)P-P:198 P-O:360 O=O:498;则反应P4(白磷)+3O2═P4O6的能量变化为( )
化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和(kJ•mol-1)P-P:198 P-O:360 O=O:498;则反应P4(白磷)+3O2═P4O6的能量变化为( )| A. | 释放1638 kJ的能量 | B. | 吸收1638 kJ的能量 | ||
| C. | 释放126 kJ的能量 | D. | 吸收126 kJ的能量 |
9.向某密闭容器中加入0.3mol A、0.1mol C和一定量的B三种气体,在一定条件下发生反应,各物质浓度随时间的变化如甲图所示[t0~t1阶段c(B)未画出].图乙为t2时刻后改变条件平衡体系中化学反应速率随时间变化的情况,四个阶段各改变一种条件并且改变的条件均不同.已知,t3~t4阶段为使用催化剂.下列说法正确的是( )
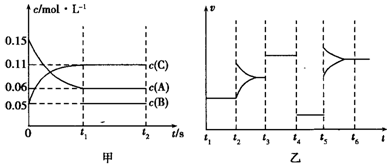

| A. | 若t1=15s,生成物C在t0~t1时间段的化学反应速率为0.004mol•L-1•s-1 | |
| B. | t4~t5阶段改变的条件为降低反应温度 | |
| C. | B的起始物质的量为0.02mol | |
| D. | t5~t6阶段可能是增大压强 |
16.下列仅能在水溶液中导电的电解质是( )
| A. | SO2 | B. | NH4Cl | C. | Na2CO3 | D. | NaCl |
6.A~G各物质间的关系如图所示,其中B、D为气体单质.则下列说法错误的是( )


| A. | 已知C的浓溶液在催化剂存在的条件下加热,能与B反应生成D,由此可以推断B的氧化性比MnO2强 | |
| B. | 反应②的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O | |
| C. | 新配制的F溶液一般需要加入铁屑和稀盐酸,前者用于防止Fe2+被空气氧化成Fe3+,后者可抑制Fe2+的水解 | |
| D. | 若反应①在常温下进行,则1 mol A在反应中能转移1 mol电子 |
13.下列说法中正确的是( )
| A. | s区都是金属元素 | B. | 所有非金属元素都在p区 | ||
| C. | 稀有气体在ds区 | D. | s区都是主族元素 |
11.某溶液中含有下列离子Na+、Fe3+、Cl-、Fe2+、Al3+ 向其中先加入足量的Na2O2,然后微热并搅拌,再加入足量的稀盐酸原溶液中离子物质的量基本不变的为( )
| A. | Al3+ | B. | Fe3+ | C. | Cl- | D. | Fe2+ | ||||
| E. | Na+ |
 .
.