题目内容
19.元素周期表有7个横行,叫周期,每一周期中元素原子的电子层数相同,元素周期表中有18列,第ⅥA族处在第16列,同一主族从上到下,元素的非金属性依次减弱(填增强或减弱).分析 元素周期表的结构:七个周期,十六个族,每一行电子层数相同,每主族元素原子最外层电子数相等,根据周期和族的分布以及元素周期表中的递变规律知识来回答.
解答 解:元素周期表的结构:7个行即七个周期,18个列,即十六个族,第ⅥA族处在第16列,每一周期中电子层数相同,同一主族从上到下,元素的非金属性依次减弱,
故答案为:7;电子层数;18;16;减弱.
点评 本题考查学生元素周期表的结构和元素性质的递变规律知识,可以根据所学内容来回答,难度不大.

练习册系列答案
相关题目
14.为除去FeCl2溶液中含有的少量FeCl3、CuCl2杂质,可选用的一种试剂是( )
| A. | 铜粉 | B. | 铁粉 | C. | 氯水 | D. | NaOH |
15.下列分子构型是直线型的为( )
| A. | C2H6 | B. | C2H4 | C. | C2H2 | D. | CO2 |
7.向明矾溶液中滴入Ba(OH)2溶液时,当SO42-沉淀完全时,铝元素的存在形式是( )
| A. | 一部分为Al(OH)3沉淀,一部分以Al3+形式存在于溶液中 | |
| B. | 一部分为Al(OH)3沉淀,一部分以-形式存在于溶液中 | |
| C. | 全部为Al(OH)3沉淀 | |
| D. | 几乎全部以AlO2-存在于溶液中 |
14.决定一定物质的量气体体积大小的主要因素是( )
| A. | 气体分子的大小 | B. | 气体分子的质量 | ||
| C. | 气体分子间距离的大小 | D. | 气体分子的组成 |
4.分别处于第二、三周期的主族元素A和B,它们的离子的电子层相差2层.已知A处于第m族;B处于第n族;A只有正化合价.则A、B原子核外电子总数分别为( )
| A. | m、n | B. | 3、7 | C. | m-2、10n | D. | m+2、n+10 |
11.Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器.其它条件相同时,在Ⅰ、Ⅱ中分别加入2molX和2molY,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?)?Z(g).则下列说法一定正确的是( )
| A. | 若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ=Ⅱ | |
| B. | 若X、Y均为气态,则平衡时气体X的转化率:Ⅰ>Ⅱ | |
| C. | 若X为固态,Y为气态,则Ⅰ、Ⅱ中从起始到平衡所需时间不相同 | |
| D. | 平衡时Ⅰ容器的体积小于VL |
9.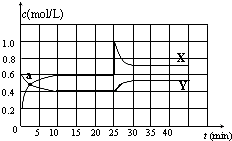 已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( )
已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( )
 已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( )
已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( )| A. | 图中的两条曲线,X是表示NO2浓度随时间的变化曲线 | |
| B. | a点时v(N2O4)=v(NO2) | |
| C. | 25min时改变了影响速率的一个因素,使得NO2转变为N2O4,该改变是将密闭容器的体积缩小,增大压强 | |
| D. | 前10min内用v(N2O4)表示的化学反应速率为0.02 mol/(L•min) |