题目内容
5.用已知浓度的NaOH溶液滴定未知浓度的盐酸,选用酚酞作指示剂,如何知道滴定到达终点?无色变粉红色且半分钟不褪去.下列操作会导致测定结果偏低的是CA.碱式滴定管未润洗就装标准液滴定
B.锥形瓶未用待测液润洗
C.读取标准液读数时,滴前平视,滴定到终点后俯视
D.滴定前碱式滴定管尖嘴处有气泡未排除,滴定后气泡消失.
分析 根据酚酞遇到酸显示无色,遇到碱溶液显示红色分析滴定终点;根据c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$分析不当操作对V(标准)×的影响,以此判断操作误差,据此分析解答.
解答 解:达到结束前,滴入酚酞的盐酸溶液为无色,当盐酸与氢氧化钠溶液恰好反应时,溶液变为粉红色,则滴定终点的现象为:无色变粉红色且半分钟不褪去;
A.锥形瓶未用待测液润洗,待测液的物质的量不变,标准液的体积不变,结果不变,故A错误;
B.酸式滴定管用蒸馏水洗后未用标准液润洗就装标准液滴定,标准液浓度偏小,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$可知c(待测)偏高,故B错误;
C.读取标准液读数时,滴前仰视,滴定到终点后俯视,造成V(标准)偏小,根据c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$可知c(待测)偏低,故C正确;
D.滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$可知c(待测)偏高,故D错误;
故答案为:无色变粉红色且半分钟不褪去; C.
点评 本题考查了中和滴定的操作方法及误差分析,题目难度中等,明确中和滴定操作方法为解答关键,注意掌握判断滴定终点的方法,能够根据实验操作对c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$的影响分析滴定误差,试题培养了学生的化学实验能力.

练习册系列答案
相关题目
15.若NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 1molCl2的体积为22.4L | |
| B. | 在0℃101KPa时,22.4L氢气中含有NA个氢原子 | |
| C. | 14g氮气中含有7NA个电子 | |
| D. | NA个CO和0.5molCH4的质量比为7:4 |
13.下列说法正确的是( )
| A. | 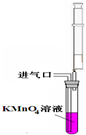 用如图所示装置测定空气中甲醛含量,若抽气速度过快会导致测定的甲醛含量偏低 | |
| B. | 溶质的溶解度越大,溶液的浓度越高,溶剂的蒸发速度越快,溶液的冷却速度越快,析出的晶体就越细小 | |
| C. | 将20g硝酸钠和17g氯化钾放入100ml烧杯中,加35mL水,并加热、搅拌,使溶液浓缩至约为原来的一半时,趁热过滤即可得到硝酸钾晶体 | |
| D. | 用移液管取液后,将移液管垂直伸入容器里面,松开食指使溶液全部流出,数秒后取出 |
20.下列说法不正确的是( )
| A. | 某芳香烃的分子式为C10H14,它不能使溴水褪色,但可使酸性KMnO4溶液褪色,且分子结构中只有一个烷基,符合条件的烃有3种 | |
| B. | 2,3-二羟基丙醛是最简单的醛糖 | |
| C. | 甲烷、甲醛、尿素都不存在同分异构体 | |
| D. | 某有机物含有C、H、O、N四种元素,其球棍模型为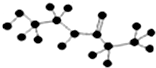 ,该有机物的结构简式为 ,该有机物的结构简式为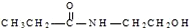 |
10.几种短周期元素的原子半径及某些化合价见下表.分析判断下列说法正确的是( )
| 元素代号 | A | B | D | E | G | I | J | K |
| 化合价 | -1 | -2 | +4 -4 | +7 -1 | +5 -3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
| A. | A的单质是一种常见的还原剂 | |
| B. | A、I、J的离子半径由大到小顺序是A>J>I | |
| C. | G元素的单质不存在同素异形体 | |
| D. | J在DB2中燃烧生成两种化合物 |
17.下列各组互为同位素的是( )
| A. | 氧气、臭氧 | B. | 重氢、超重氢 | C. | 纯碱、苏打 | D. | 乙酸、甲酸 |
14.环丙叉环丙烷(A)由于其特殊的电子结构,一直受到结构和理论化学家的注意,由于缺乏有效的合成途径,一度延缓对其反应的研究,直到1993年出现了可以大量制备的方法.根据下列转化,判断下列说法正确的是( )


| A. | A的所有原子都在一个平面内 | B. | 反应①是加成反应 | ||
| C. | 反应②是消去反应 | D. | A的二取代产物只有1种 |
15.下列离子中,电子数大于质子数且质子数大于中子数的是( )
| A. | H3O+ | B. | Li+ | C. | OD- | D. | OH- |
 .
.