题目内容
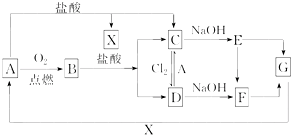 已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.
已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.(1)写出A、C、F、G的化学式
A
(2)保存C溶液时要加固体A的原因:
(3)写出下列转化的化学方程式.
①E→F:
写出下列转化的离子方程式
②C→D:
③B→C+D:
④D→C:
考点:无机物的推断
专题:推断题
分析:A是一种常见金属,F是一种红褐色沉淀,由转化关系可知F为Fe(OH)3,A为Fe,Fe与氧气反应生成B为Fe3O4,四氧化三铁与盐酸反应得到氯化亚铁与氯化铁,故Fe与盐酸反应得到X为氢气、C为FeCl2,可推知E为Fe(OH)2、D为FeCl3,G为Fe2O3,据此解答.
解答:
解:A是一种常见金属,F是一种红褐色沉淀,由转化关系可知F为Fe(OH)3,A为Fe,Fe与氧气反应生成B为Fe3O4,四氧化三铁与盐酸反应得到氯化亚铁与氯化铁,故Fe与盐酸反应得到X为氢气、C为FeCl2,可推知E为Fe(OH)2、D为FeCl3,G为Fe2O3,
(1)由上述分析可知,A为Fe,C为FeCl2,F为Fe(OH)3,G为Fe2O3,
故答案为:Fe;FeCl2;Fe(OH)3;Fe2O3.
(2)FeCl2易被空气中氧气氧化,保存FeCl2溶液时加固体Fe,防止Fe2+被氧气氧化,
故答案为:防止Fe2+被氧气氧化;
(3)①E→F的反应是氢氧化亚铁被氧气氧化生成氢氧化铁,反应化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
②C→D的反应离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
③B→C+D的反应是四氧化三铁和盐酸反应生成氯化铁,氯化亚铁和水,反应的离子方程式为:Fe3O4+8H+=Fe2++Fe3++4H2O;
故答案为:Fe3O4+8H+=Fe2++Fe3++4H2O;
④D→C是铁和氯化铁溶液反应生成氯化亚铁,反应的离子方程式为:2Fe3++Fe=3Fe2+;
故答案为:2Fe3++Fe=3Fe2+.
(1)由上述分析可知,A为Fe,C为FeCl2,F为Fe(OH)3,G为Fe2O3,
故答案为:Fe;FeCl2;Fe(OH)3;Fe2O3.
(2)FeCl2易被空气中氧气氧化,保存FeCl2溶液时加固体Fe,防止Fe2+被氧气氧化,
故答案为:防止Fe2+被氧气氧化;
(3)①E→F的反应是氢氧化亚铁被氧气氧化生成氢氧化铁,反应化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
②C→D的反应离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
③B→C+D的反应是四氧化三铁和盐酸反应生成氯化铁,氯化亚铁和水,反应的离子方程式为:Fe3O4+8H+=Fe2++Fe3++4H2O;
故答案为:Fe3O4+8H+=Fe2++Fe3++4H2O;
④D→C是铁和氯化铁溶液反应生成氯化亚铁,反应的离子方程式为:2Fe3++Fe=3Fe2+;
故答案为:2Fe3++Fe=3Fe2+.
点评:本题考查无机物推断,涉及Fe元素单质化合物的性质及转化,物质的颜色是推断突破口,再结合转化关系推断各物质,掌握元素化合物的性质是解题的关键,题目难度中等.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
下列有关铁元素的叙述中正确的是( )
| A、铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3 |
| B、氢氧化铁可以由相应的物质通过化合反应而制得 |
| C、氢氧化铁与氢碘酸反应:Fe(OH)3+3HI═FeI3+3H2O |
| D、铁元素位于周期表中第4周期第VIIIB族 |
下列溶液一定呈中性的是( )
| A、pH=7的溶液 |
| B、c(H+)=c(OH-)的溶液 |
| C、滴加酚酞,颜色未变红的溶液 |
| D、酸与碱恰好完全反应生成正盐的溶液 |


 的单体的结构简式:
的单体的结构简式: