题目内容
如图是一个制取氯气并以氯气为原料进行某个特定反应研究的装置.
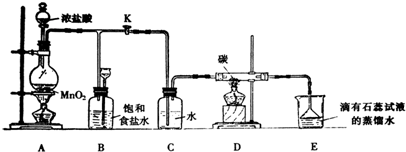
(1)实验开始时,先点燃A处的酒精灯,打开K,使Cl2充满整个装置,再点燃D处酒精灯,然后连接上E装置;E处石蕊试液先变红然后渐变为无色,同时漏斗中的液面略有上升,则产生颜色变化的原因是 .
a.反应中产生CO2的缘故 b.反应中产生HCl的缘故
c.反应中产生HCl并有Cl2溶于水 d.反应中同时有CO2、HCl产生的缘故
D处反应的化学方程式为 .
(2)装置C的作用是 .
(3)若将E处中的液体改为澄清石灰水,反应过程中的现象为 .
a.有白色沉淀产生 b.先生成白色沉淀而后沉淀消失
c.无明显现象 d.开始无沉淀,然后产生白色沉淀
(4)当反应结束后关闭K,移去A处酒精灯,由于余热作用,A处仍有Cl2产生,此时B中现象为 ,B的作用是 .
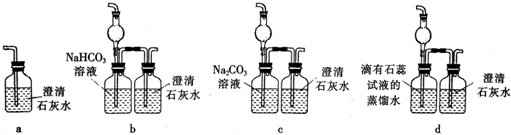
(5)E装置无法确认D处反应中有CO2产生,为了证明CO2的存在,要对E装置进行改变,下列装置符合要求的是 .

(1)实验开始时,先点燃A处的酒精灯,打开K,使Cl2充满整个装置,再点燃D处酒精灯,然后连接上E装置;E处石蕊试液先变红然后渐变为无色,同时漏斗中的液面略有上升,则产生颜色变化的原因是
a.反应中产生CO2的缘故 b.反应中产生HCl的缘故
c.反应中产生HCl并有Cl2溶于水 d.反应中同时有CO2、HCl产生的缘故
D处反应的化学方程式为
(2)装置C的作用是
(3)若将E处中的液体改为澄清石灰水,反应过程中的现象为
a.有白色沉淀产生 b.先生成白色沉淀而后沉淀消失
c.无明显现象 d.开始无沉淀,然后产生白色沉淀
(4)当反应结束后关闭K,移去A处酒精灯,由于余热作用,A处仍有Cl2产生,此时B中现象为
(5)E装置无法确认D处反应中有CO2产生,为了证明CO2的存在,要对E装置进行改变,下列装置符合要求的是

考点:氯气的实验室制法,氯、溴、碘的性质实验
专题:实验题
分析:(1)根据浓盐酸的性质及制取氯气的反应条件以及D装置发生的反应分析,根据盐酸和次氯酸的性质分析;氯气有强氧化性,碳有还原性,在加热条件下氯气和水、碳发生氧化还原反应生成氯化氢和二氧化碳;紫色石蕊遇酸变红色,次氯酸有漂白作用;
(2)根据D装置中发生的反应分析,C装置为D装置提供水蒸气;
(3)氯气、氯化氢与氢氧化钙反应,无明显现象;
(4)根据B装置内气体的压强变化分析液面变化,关闭K撤去酒精灯,余热反应继续进行,生成的氯气使B中压强增大,饱和食盐水被压入长颈漏斗中;
(5)确认D处反应中有CO2产生,需用澄清的石灰水变浑浊验证,需除去二氧化碳中的氯化氢、氯气,且不能生成二氧化碳;
(2)根据D装置中发生的反应分析,C装置为D装置提供水蒸气;
(3)氯气、氯化氢与氢氧化钙反应,无明显现象;
(4)根据B装置内气体的压强变化分析液面变化,关闭K撤去酒精灯,余热反应继续进行,生成的氯气使B中压强增大,饱和食盐水被压入长颈漏斗中;
(5)确认D处反应中有CO2产生,需用澄清的石灰水变浑浊验证,需除去二氧化碳中的氯化氢、氯气,且不能生成二氧化碳;
解答:
解:(1)在加热条件下,浓盐酸和二氧化锰反应制取氯气,浓盐酸具有挥发性,所以制取的氯气中有氯化氢气体,氯气有强氧化性,碳有还原性,在加热条件下氯气和水、碳发生氧化还原反应生成氯化氢和二氧化碳,反应方程式为:2Cl2+C+2H2O
CO2+4HCl,氯化氢极易溶于水,紫色石蕊遇酸变红色,氯气也能溶于水,氯气和水反应生成盐酸和次氯酸,次氯酸有漂白作用,所以在E处,紫色石蕊纸的颜色由紫色变为红色,再变为无色,同时漏斗中的液面略有上升,
故答案为:C;2Cl2+C+2H2O
CO2+4HCl;
(2)A装置产生了氯气,D装置中发生反应2Cl2+C+2H2O
CO2+4HCl,D装置反应需提供水蒸气,C装置为D处所需水蒸气,
故答案为:提供水蒸汽;
(3)剩余的氯气在E装置中和水反应生成盐酸和次氯酸,氯化氢、次氯酸和澄清石灰水反应都生成可溶性的盐和水,所以反应过程无现象无白色沉淀生成,
故答案为:C;
(4)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,气体通过导管进入B装置,导致B装置中气体的压强增大,大于大气压,迫使瓶中液面下降,长颈漏斗内液面上升,B的作用是储存多余氯气,防止污染,
故答案为:B中液体被压入长颈漏斗中;储存多余氯气,防止污染;
(5)因通入D装置的气体中含有氯气、氯化氢、二氧化碳,现需除去氯气和氯化氢,且除去这两种气体过程中不能产生二氧化碳,装置a氯气、氯化氢、二氧化碳一同通入无法确认D处反应中有CO2产生;b装置氯化氢与碳酸氢钠反应生成二氧化碳,无法确认D处反应中有CO2产生;装置C中碳酸钠与氯化氢反应生成二氧化碳,无法确认D处反应中有CO2产生;少量氯气能溶于水,氯化氢极易溶于水,二氧化碳混有氯化氢,二氧化碳在水中不溶,用水可除去氯气和氯化氢两种气体,多余的气体与澄清石灰水作用变浑浊,能确认D处反应中有CO2产生,
故答案为:d;
| ||
故答案为:C;2Cl2+C+2H2O
| ||
(2)A装置产生了氯气,D装置中发生反应2Cl2+C+2H2O
| ||
故答案为:提供水蒸汽;
(3)剩余的氯气在E装置中和水反应生成盐酸和次氯酸,氯化氢、次氯酸和澄清石灰水反应都生成可溶性的盐和水,所以反应过程无现象无白色沉淀生成,
故答案为:C;
(4)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,气体通过导管进入B装置,导致B装置中气体的压强增大,大于大气压,迫使瓶中液面下降,长颈漏斗内液面上升,B的作用是储存多余氯气,防止污染,
故答案为:B中液体被压入长颈漏斗中;储存多余氯气,防止污染;
(5)因通入D装置的气体中含有氯气、氯化氢、二氧化碳,现需除去氯气和氯化氢,且除去这两种气体过程中不能产生二氧化碳,装置a氯气、氯化氢、二氧化碳一同通入无法确认D处反应中有CO2产生;b装置氯化氢与碳酸氢钠反应生成二氧化碳,无法确认D处反应中有CO2产生;装置C中碳酸钠与氯化氢反应生成二氧化碳,无法确认D处反应中有CO2产生;少量氯气能溶于水,氯化氢极易溶于水,二氧化碳混有氯化氢,二氧化碳在水中不溶,用水可除去氯气和氯化氢两种气体,多余的气体与澄清石灰水作用变浑浊,能确认D处反应中有CO2产生,
故答案为:d;
点评:本题考查实验室制取氯气及其物质的性质,明确反应原理是解答本题的关键,注意结合题干新信息、灵活运用物质之间的反应,题目难度中等.

练习册系列答案
相关题目
已知相同条件下,HClO的电离常数小于H2CO3的第一级电离常数(Ka1)大于H2CO3的第二级电离常数(Ka2).为了提高氯水中HClO的浓度,可行的是( )
| A、通入HCl(g) |
| B、加入NaHCO3(s) |
| C、加入H2O |
| D、加入NaOH(s) |
将①氢气;②氧气;③甲烷三种气体分别盛放在三个容器中,并保持三个容器内气体的温度和密度均相等,这三种气体压强的大小关系是( )
| A、①>②=③ |
| B、①>③>② |
| C、①<②<③ |
| D、①<③<② |
在理论上不能用于设计原电池的化学反应是( )
| A、HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H<0 |
| B、2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H<0 |
| C、Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H<0 |
| D、2H2(g)+O2(g)═2H2O(l)△H<0 |
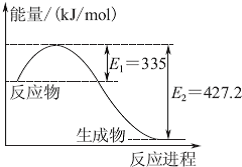 (1)已知:C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
(1)已知:C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol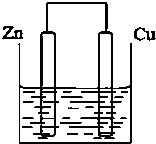 将质量相等的锌片和铜片用导线相连浸500mL硫酸铜溶液中构成如图的装置.
将质量相等的锌片和铜片用导线相连浸500mL硫酸铜溶液中构成如图的装置. 已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.
已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.