题目内容
 在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.3mol,则此反应的平均速率可表示为
在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.3mol,则此反应的平均速率可表示为B. v (H2O)=0.01 mol·L-1·s-1
C.v (NO)=0.09 mol·L-1·min-1
D.v (O2)=0.05mol·L-1·min-1

 阅读快车系列答案
阅读快车系列答案以下是一些物质的熔沸点数据(常压):
|
|
钾 |
钠 |
Na2CO3 |
金刚石 |
石墨 |
|
熔点(℃) |
63.65 |
97.8 |
851 |
3550 |
3850 |
|
沸点(℃) |
774 |
882.9 |
1850(分解产生CO2) |
---- |
4250 |
金属钠和CO2在常压、890℃发生如下反应:4 Na(g)+ 3CO2(g) 2 Na2CO3(l) + C(s,金刚石) △H=-1080.9kJ/mol
2 Na2CO3(l) + C(s,金刚石) △H=-1080.9kJ/mol
(1)若反应在10L密闭容器、常压下进行,温度由890℃升高到1860℃,若反应时间为10min, 金属钠的物质的量减少了0.2mol,则10min内CO2的平均反应速率为 。
(2)高压下有利于金刚石的制备,理由是 。
(3)由CO2(g)+ 4Na(g)=2Na2O(s)+ C(s,金刚石) △H=-357.5kJ/mol;则Na2O固体与C(金刚石)反应得到Na(g)和液态Na2CO3(l)的热化学方程式 。
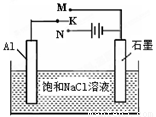
(4)下图开关K接M时,石墨电极反应式为 。

(5)请运用原电池原理设计实验,验证Cu2+、Ag+氧化性的强弱。
在方框内画出实验装置图,要求用烧杯和盐桥(在同一烧杯中,
电极与溶液含相同的金属元素),并标出外电路电子流向。

以下是一些物质的熔沸点数据(常压):
|
|
钾 |
钠 |
Na2CO3 |
金刚石 |
石墨 |
|
熔点(℃) |
63.65 |
97.8 |
851 |
3550 |
3850 |
|
沸点(℃) |
774 |
882.9 |
1850(分解产生CO2) |
---- |
4250 |
金属钠和CO2在常压、890℃发生如下反应:
4 Na(g)+ 3CO2(g) 2
Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
2
Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
(1)上述反应的平衡常数表达式为 ;若4v正(Na)=3v逆(CO2),反应是否达到平衡 (选填“是”或“否”)。
(2)若反应在10L密闭容器、常压下进行,温度由890℃升高到1680℃,若反应时间为10min, 金属钠的物质的量减少了0.20mol,则10min里CO2的平均反应速率为 。
(3)高压下有利于金刚石的制备,理由是 。
(4)由CO2(g)+4Na(g)=2Na2O(s)+C(s,金刚石) △H=-357.5kJ/mol;则Na2O固体与C(金刚石)反应得到Na(g)和液态Na2CO3(l)的热化学方程式 。
(5)下图开关K接M时,石墨作 极,电极反应式为 。K接N一段时间后测得有0.3mol电子转移,作出y随x变化的图象〖x—代表n(H2O)消耗,y—代表n[Al(OH)3],反应物足量,标明有关数据〗

 在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.3mol,则此反应的平均速率可表示为
在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.3mol,则此反应的平均速率可表示为 4NO (g)+6H2O(g)是工业制备硝酸的重要反应,此反应在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此时间内,若用NO的浓度变化来表示此反应的速率,则v(NO)应为
4NO (g)+6H2O(g)是工业制备硝酸的重要反应,此反应在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此时间内,若用NO的浓度变化来表示此反应的速率,则v(NO)应为


