��Ŀ����
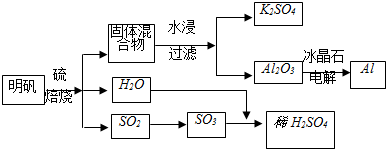
�������ף���ѧʽ��POCl3����һ����Ҫ�Ĺ�ҵ����ԭ�ϣ��������뵼����Ӽ������άԭ�ϣ��Ȼ�ˮ�ⷨ�ǹ�ҵ���Ʊ��������ij��÷��������������£�
�����Ȼ����뷴Ӧ���У�ͨ��������ͬʱ�μ�ˮ���ü�������������105��109��ʹ��Ӧ���ڷ�Ӧ�����������������������ٻ����뷴Ӧ���У�����ͨ�������������Ȼ��д���������ף���������Ӧ��ɫ���ף��������ײд�����0.2%����ʱ������������������Ϊ�������׳�Ʒ
��1���Ȼ�ˮ�ⷨ�����������Ļ�ѧ����ʽΪ
��2���Ȼ�ˮ�ⷨ������������ʱ����������ף���ҪΪH3PO3��H3PO4�ȣ���ˮ����֪H3PO3��һ�ֵ���ɫ���壬������ˮ
��H3PO3�У�PԪ�صĻ��ϼ�Ϊ
��ǡ���к�20mL H3PO3��Һ��ҪͬŨ�ȵ�NaOH��Һ40mL��д�������εĻ�ѧʽ ��ʱ��Һ�������ԣ������ӷ���ʽ��ʾ��Һ�Լ��Ե�ԭ��
�۴�����ˮʱ���������м�������Ư�ۣ��ڼ�����ʯ�ҵ���pH����Ԫ��ת��Ϊ����Ƴ��������գ�����Ư�۵������� ��д���˹��̵Ļ�ѧ����ʽ ��������ķ�ˮ��c��PO43-��=4��10-7mol?L-��Һ��C��Ca2+��= mol?L-1�� Ksp[Ca3��PO4��2]=2��10-29��
��3����ҵ�ϳ��õ�ⱥ��ʳ��ˮ�ķ��������������ͼΪ���ӽ���Ĥ����ⱥ��ʳ��ˮʾ��ͼ���������������������� NaOH��Һ�ij���Ϊ ������ĸ�����Ʊ���ʳ��ˮ�Ľ���Ϊ ������ĸ����������Ӧʹ�õ�Һ���� ��
�����Ȼ����뷴Ӧ���У�ͨ��������ͬʱ�μ�ˮ���ü�������������105��109��ʹ��Ӧ���ڷ�Ӧ�����������������������ٻ����뷴Ӧ���У�����ͨ�������������Ȼ��д���������ף���������Ӧ��ɫ���ף��������ײд�����0.2%����ʱ������������������Ϊ�������׳�Ʒ
��1���Ȼ�ˮ�ⷨ�����������Ļ�ѧ����ʽΪ
��2���Ȼ�ˮ�ⷨ������������ʱ����������ף���ҪΪH3PO3��H3PO4�ȣ���ˮ����֪H3PO3��һ�ֵ���ɫ���壬������ˮ
��H3PO3�У�PԪ�صĻ��ϼ�Ϊ
��ǡ���к�20mL H3PO3��Һ��ҪͬŨ�ȵ�NaOH��Һ40mL��д�������εĻ�ѧʽ
�۴�����ˮʱ���������м�������Ư�ۣ��ڼ�����ʯ�ҵ���pH����Ԫ��ת��Ϊ����Ƴ��������գ�����Ư�۵�������
��3����ҵ�ϳ��õ�ⱥ��ʳ��ˮ�ķ��������������ͼΪ���ӽ���Ĥ����ⱥ��ʳ��ˮʾ��ͼ����������������������

���㣺���ԭ��,���ܵ���ʵ��ܽ�ƽ�⼰����ת���ı���
ר�⣺����ƽ������Һ��pHר��,�绯ѧר��
��������1���Ȼ�ˮ�ⷨ�����������������
��2���ٸ��ݻ��ϼ۹������Ԫ�صĻ��ϼۣ�
����ͼӦ�����κ�ˮ�����������ӵ�ˮ�����Ksp[Ca3��PO4��2]=2.0��10-33���㣻
�۸��ݴ�����Ƶ�����������д����ʽ������Ksp[Ca3��PO4��2]=2.0��10-29���㣻
��3����ⱥ��ʳ��ʱ����������Cl-��OH-�ŵ磬Cl-�ķŵ�����ǿ��OH-�����������ķ���ʽΪ��2Cl--2e-�TCl2����������2H++2e-�TH2����H2��NaOH��������NaOH��Һ�ij���Ϊa��Cl2�����������Ʊ���ʳ��ˮ���������룬Ҫ����Cl2��Ҫ�����Ը���������Ը������
��2���ٸ��ݻ��ϼ۹������Ԫ�صĻ��ϼۣ�
����ͼӦ�����κ�ˮ�����������ӵ�ˮ�����Ksp[Ca3��PO4��2]=2.0��10-33���㣻
�۸��ݴ�����Ƶ�����������д����ʽ������Ksp[Ca3��PO4��2]=2.0��10-29���㣻
��3����ⱥ��ʳ��ʱ����������Cl-��OH-�ŵ磬Cl-�ķŵ�����ǿ��OH-�����������ķ���ʽΪ��2Cl--2e-�TCl2����������2H++2e-�TH2����H2��NaOH��������NaOH��Һ�ij���Ϊa��Cl2�����������Ʊ���ʳ��ˮ���������룬Ҫ����Cl2��Ҫ�����Ը���������Ը������
���
�⣺��1���Ȼ�ˮ�ⷨ�����������������ᣬ��ѧ����ʽΪ��PCl3+H2O+Cl2=POCl3+2HCl���ʴ�Ϊ��PCl3+H2O+Cl2=POCl3+2HCl��
��2����H3PO3�У�H��+1�ۣ�O��-2�ۣ����ݻ��ϼ۹���P��+3�ۣ��ʴ�Ϊ��+3�ۣ�
����ͼӦ�����κ�ˮ���������к���2���ǻ������ڶ�Ԫ�ᣬ������������Ԫ�ᣬ20mL H3PO3��Һ��ҪͬŨ�ȵ�NaOH��Һ40mL�������������������������Ƶķ�Ӧ����ʽΪ��H3PO3+2NaOH=Na2HPO3+2H2O����ʱ��Һ�������ԣ�HPO32-+H2O?HPO3-+OH-���ʴ�Ϊ��H3PO3+2NaOH=Na2HPO3+2H2O��HPO32-+H2O?HPO3-+OH-��
�۴�����ˮʱ���������м�������Ư�ۣ�����ˮ�е�H3PO3����Ϊ���ᣬ������ʯ�ҵ���pH��ʹ��ת��Ϊ����ƣ������ķ�ӦΪ��2H3PO3+Ca��ClO��2+2Ca��OH��2=Ca3��PO4��2+2HCl+4H2O��
Ksp[Ca3��PO4��2]=c3��Ca2+����c2��PO43-��=c3��Ca2+������4.0��10-7��2=2.0��10-29��c��Ca2+��=6.3��10-6mol?L-1���ʴ�Ϊ��2H3PO3+Ca��ClO��2+2Ca��OH��2=Ca3��PO4��2+2HCl+4H2O��6.3��10-6��
��3������ͼװ�ÿ�֪�����������������ӷŵ������������缫��ӦΪ��2Cl--2e-�TCl2���������������������ӷŵ�����������ˮ����ƽ�������������������Ũ��������������������Һ��NaOH��Һ�ij���Ϊa��Cl2������������װ��ͼ������֪���Ʊ���ʳ��ˮ���������룬������Ϊd��Ҫ����Cl2��Ҫ�����Ը���������Ը������������Ũ������
�ʴ�Ϊ��������a��d��Ũ���ᣮ
��2����H3PO3�У�H��+1�ۣ�O��-2�ۣ����ݻ��ϼ۹���P��+3�ۣ��ʴ�Ϊ��+3�ۣ�
����ͼӦ�����κ�ˮ���������к���2���ǻ������ڶ�Ԫ�ᣬ������������Ԫ�ᣬ20mL H3PO3��Һ��ҪͬŨ�ȵ�NaOH��Һ40mL�������������������������Ƶķ�Ӧ����ʽΪ��H3PO3+2NaOH=Na2HPO3+2H2O����ʱ��Һ�������ԣ�HPO32-+H2O?HPO3-+OH-���ʴ�Ϊ��H3PO3+2NaOH=Na2HPO3+2H2O��HPO32-+H2O?HPO3-+OH-��
�۴�����ˮʱ���������м�������Ư�ۣ�����ˮ�е�H3PO3����Ϊ���ᣬ������ʯ�ҵ���pH��ʹ��ת��Ϊ����ƣ������ķ�ӦΪ��2H3PO3+Ca��ClO��2+2Ca��OH��2=Ca3��PO4��2+2HCl+4H2O��
Ksp[Ca3��PO4��2]=c3��Ca2+����c2��PO43-��=c3��Ca2+������4.0��10-7��2=2.0��10-29��c��Ca2+��=6.3��10-6mol?L-1���ʴ�Ϊ��2H3PO3+Ca��ClO��2+2Ca��OH��2=Ca3��PO4��2+2HCl+4H2O��6.3��10-6��
��3������ͼװ�ÿ�֪�����������������ӷŵ������������缫��ӦΪ��2Cl--2e-�TCl2���������������������ӷŵ�����������ˮ����ƽ�������������������Ũ��������������������Һ��NaOH��Һ�ij���Ϊa��Cl2������������װ��ͼ������֪���Ʊ���ʳ��ˮ���������룬������Ϊd��Ҫ����Cl2��Ҫ�����Ը���������Ը������������Ũ������
�ʴ�Ϊ��������a��d��Ũ���ᣮ
���������⿼����ԭ����ԭ��Ӧ���Լ����ܵ���ʵ��ܽ�ƽ���Լ�����ת���ı��ʣ���ⷴӦ�缫�ж��ǽ���ؼ�����Ŀ�ѶȽϴ�

��ϰ��ϵ�д�
�����Ŀ
��˵��������������ʵ��ǣ�������
| A����ʳ���Գ���ˮƿ�ڵ�ˮ�� |
| B��������Һ��ˮϡ�ͺ�������Ũ���½� |
| C��pH=2�Ĵ�����Һϡ��1000����pHС��5 |
| D����ŨH2SO4�ʹ����ƹ��干�ȿ��Ƶô��� |
�����йػ�ѧ�����ʾ��ȷ���ǣ�������
| A���������辧��ķ���ʽΪ��SiO2 | ||||
B��CO2�ĵ���ʽΪ�� | ||||
C�����ӽṹʾ��ͼΪ�� �����ȿɱ�ʾ �����ȿɱ�ʾ
| ||||
| D��������ĽṹʽΪ��H-Cl-O |
����������ȷ���ǣ�������
| A����ϩ�ͱ�����ʹ��ˮ��ɫ���ʲ�������ˮ������ϩ�ͱ����� |
| B��HNO3���뱽���ױ������͡���ά�ص��л������Ҫ��Ӧ������Ũ���������� |
| C���������Ƶ�������ͭ����Һһ���Լ����ɼ����Ҵ�����ȩ�����ᡢ�������� |
| D����������KMnO4��Һ��������÷ֲ㣬�²�Һ��Ϊ��ɫ |
 ��ȡ
��ȡ ��
��
 ����Ӧ�Ļ�ѧ����ʽΪ��
����Ӧ�Ļ�ѧ����ʽΪ��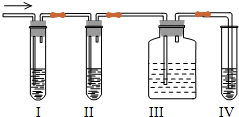
 ij����M�����ԭ������Ϊ112.4�������Ȼ��ﻯѧʽΪMClx����a g�Ȼ�������ˮ���Ƴ�0.2mol?L-1����Һ1L���ö��Ե缫��⣬A�۵���������0.0539g��B�۵���������0.0281g����
ij����M�����ԭ������Ϊ112.4�������Ȼ��ﻯѧʽΪMClx����a g�Ȼ�������ˮ���Ƴ�0.2mol?L-1����Һ1L���ö��Ե缫��⣬A�۵���������0.0539g��B�۵���������0.0281g����