题目内容
有一包白色粉末,其中可能含有Ba(NO3)2、CaCl2、K2CO3,将部分粉末加入水中,振荡,有白色沉淀生成,向悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;往所得溶液中滴入AgNO3溶液,有白色沉淀生成.根据上述实验现象,下列判断正确的是( )
| A、该白色粉末中肯定含有Ba(NO3)2、CaCl2、K2CO3 |
| B、该白色粉末中可能含有CaCl2 |
| C、该白色粉末中可能含有Ba(NO3)2 |
| D、该白色粉末中肯定含有Ba(NO3)2、K2CO3 |
考点:几组未知物的检验
专题:
分析:依据实验过程中的现象分析判断:
(1)将部分粉末加入水中,振荡,有白色沉淀生成,说明含有能生成白色沉淀的物质;
(2)向(1)的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生,白色沉淀可以是碳酸钡或碳酸钙;
(3)取少量(2)的溶液商入AgNO3溶液,有白色沉淀生成.证明含有氯离子,混合物中一定含有CaCl2,以此解答该题.
(1)将部分粉末加入水中,振荡,有白色沉淀生成,说明含有能生成白色沉淀的物质;
(2)向(1)的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生,白色沉淀可以是碳酸钡或碳酸钙;
(3)取少量(2)的溶液商入AgNO3溶液,有白色沉淀生成.证明含有氯离子,混合物中一定含有CaCl2,以此解答该题.
解答:
解:(1)将部分粉末加入水中,振荡,有白色沉淀生成,说明含有能生成白色沉淀的物质;
(2)向(1)的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生,白色沉淀可以是碳酸钡或碳酸钙;
(3)取少量(2)的溶液商入AgNO3溶液,有白色沉淀生成.证明含有氯离子,混合物中一定含有CaCl2,
所以原白色粉末中肯定含有CaCl2、K2CO3,可能含有Ba(NO3)2,
故选C.
(2)向(1)的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生,白色沉淀可以是碳酸钡或碳酸钙;
(3)取少量(2)的溶液商入AgNO3溶液,有白色沉淀生成.证明含有氯离子,混合物中一定含有CaCl2,
所以原白色粉末中肯定含有CaCl2、K2CO3,可能含有Ba(NO3)2,
故选C.
点评:本题考查了常见物质的性质应用和鉴别,为高频考点,侧重于学生的分析能力的考查,注意抓住物质的特征性质是解答本题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法中,正确的是( )
A、某原子(6个电子、7个中子)的化学符号是
| ||
| B、H2O和CH4分子中具有相同的质子数和原子数 | ||
| C、D和T是氢元素的两种不同的核素 | ||
| D、稀有气体的原子最外层达到稳定结构,故都不能与别的物质发生反应 |
下列化学用语正确的是( )
A、乙酸根离子的结构式: |
| B、3-甲基1-丁烯的结构简式:(CH3)2CHCH═CH2 |
| C、乙酸的结构简式C2H4O2 |
D、醛基的电子式: |
下列实验操作正确的是( )
| A、分液时,上下层液体均从下口放出 |
| B、蒸馏时忘记放碎瓷片可停止加热,冷却后补加 |
| C、蒸发结晶时,应将蒸发皿中的溶液全部蒸干 |
| D、过滤时,为加快过滤速度可搅拌漏斗内的液体 |
下列关于MgO和Al2O3性质和用途的说法不符合事实的是( )
| A、都可与盐酸反应 |
| B、都难溶于水 |
| C、都常用作耐火材料 |
| D、都可与氢氧化钠溶液反应 |
室温下对浓度,体积均相同的盐酸和醋酸溶液分别采取下列措施,有关叙述不正确的是( )
| A、醋酸溶液的PH值较大 |
| B、完全中和两溶液,需要浓度相同NaOH溶液的体积相等 |
| C、两者稀释相同倍数后,pH值变化相等 |
| D、加足量的锌充分反应后,两溶液中产生的氢气一样多 |
根据有机化合物的命名原则,下列命名正确的是( )
A、 3-甲基-1?3-丁二烯 |
B、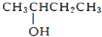 2-羟羟基丁烷 |
C、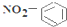 硝基苯 |
D、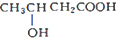 3-羟基丁酸 |