题目内容
13.写出离子方程式:①氢氧化钡与硫酸铜反应:Ba2++SO42-+2OH-+Cu2+═BaSO4↓+Cu(OH)2↓
②少量CO2通入澄清石灰水中:Ca2++CO2+2OH-=CaCO3↓+H2O.
分析 ①硫酸铜溶液与氢氧化钡反应生成硫酸钡和氢氧化铜;
②反应生成碳酸钙和水.
解答 解:①硫酸铜溶液与氢氧化钡反应生成硫酸钡和氢氧化铜,离子方程式:Ba 2++SO42-+2OH-+Cu2+═BaSO4↓+Cu(OH)2↓;
故答案为:Ba 2++SO42-+2OH-+Cu2+═BaSO4↓+Cu(OH)2↓;
②少量CO2通入澄清石灰水中生成碳酸钙和水,离子反应为Ca2++CO2+2OH-=CaCO3↓+H2O,
故答案为:Ca2++CO2+2OH-=CaCO3↓+H2O.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
7.下述实验能达到预期目的是编号( )
| 实验内容 | 实验目的 | |
| A | 向1mL 1%的NaOH溶液中加入2mL 2%的CuSO4溶液,振荡后再加入0.5mL有机物X,加热煮沸后未出现砖红色沉淀 | 验证X结构中不含有醛基 |
| B | 在混有少量苯酚的苯中滴加足量溴水,充分振荡后过滤 | 除去苯中少量的苯酚 |
| C | 溴乙烷与NaOH溶液加热至不再分层,冷却后加稀硝酸至酸性,再滴加AgNO3溶液 | 验证卤素原子为溴原子 |
| D | 将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中 | 检验气体中含有乙烯 |
| A. | A | B. | B | C. | C | D. | D |
4.甲醇是重要的化工原料,又是一种可再生能源,具有广泛的开发和应用前景.
(1)已知反应CO(g)+2H2(g)?CH3OH(g)△H=-99kJ.mol-1中的相关化学键键能如下:
则x=1076.
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:CO(g)+2H2(g)$\stackrel{催化剂}{?}$ CH3OH(g)△H1<0,CO在不同温度下的平衡转化率(α)与压强的关系如图1所示.
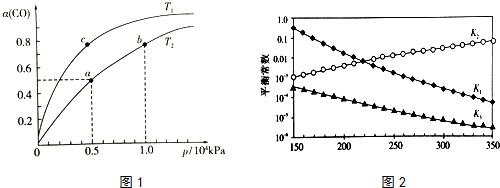
①a、b两点的反应速率:v(a)<v(b)(填“>”“<”或“=”).
②T1<T2(填“>”“<”或“=”),原因是该反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2.该反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是bc(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
④图中a点的平衡常数KP=1.6×10-7(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(3)利用合成气(主要成分为CO和H2)合成甲醇,发生主要反应如下:
Ⅰ:CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1
Ⅱ:CO2(g)+H2(g)$\stackrel{催化剂}{?}$CO(g)+H2O(g)△H2
Ⅲ:CO2(g)+3H2(g)$\stackrel{催化剂}{?}$CH3OH(g)+H2O(g)△H3
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化曲线如图2所示.
则△H1<△H3(填“>”、“<”、“=”),理由是由图可知,随着温度升高,K2减小,则△H2>0,根据盖斯定律又得△H3=△H1+
△H2,所以△H1<△H3..
(1)已知反应CO(g)+2H2(g)?CH3OH(g)△H=-99kJ.mol-1中的相关化学键键能如下:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(KJ•mol-1) | 436 | 343 | x | 465 | 413 |
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:CO(g)+2H2(g)$\stackrel{催化剂}{?}$ CH3OH(g)△H1<0,CO在不同温度下的平衡转化率(α)与压强的关系如图1所示.

①a、b两点的反应速率:v(a)<v(b)(填“>”“<”或“=”).
②T1<T2(填“>”“<”或“=”),原因是该反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2.该反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是bc(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
④图中a点的平衡常数KP=1.6×10-7(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(3)利用合成气(主要成分为CO和H2)合成甲醇,发生主要反应如下:
Ⅰ:CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1
Ⅱ:CO2(g)+H2(g)$\stackrel{催化剂}{?}$CO(g)+H2O(g)△H2
Ⅲ:CO2(g)+3H2(g)$\stackrel{催化剂}{?}$CH3OH(g)+H2O(g)△H3
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化曲线如图2所示.
则△H1<△H3(填“>”、“<”、“=”),理由是由图可知,随着温度升高,K2减小,则△H2>0,根据盖斯定律又得△H3=△H1+
△H2,所以△H1<△H3..
1.工业上用生锈的Fe粉和Cu粉的混合物制备CuSO4•5H2O和FeSO4•(NH4)2SO4•6H2O的工艺流程如图1所示.
已知:①几种物质的溶解度(g/100gH2O)如表所示.
②溶液pH>4时,Fe2+容易被氧化.
请回答:
(1)过滤所用的主要玻璃仪器为玻璃棒、漏斗、烧杯.
(2)溶液1中的主要溶质为FeSO4、H2SO4(填化学式).
(3)进行操作2时,从溶液中析出晶体后,需趁热过滤,原因为减小硫酸亚铁和硫酸铵的析出使得FeSO4•(NH4)2SO4•6H2O晶体更纯.
(4)FeSO4•(NH4)2SO4•6H2O用适量稀硫酸洗涤,而不是用水洗涤的原因为抑制亚铁离子和铵根离子的水解,防止亚铁离子被氧化.
(5)称取2.50gCuSO4•5H2O样品,灼烧过程中样品质量随温度(T)变化的曲线如图2所示.
①120℃所的固体,继续加热至258℃时失水,所发生反应的化学方程式为CuSO4•H2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+H2O.
②900℃时剩余固体只有一种铜的氧化物,其化学式为Cu2O.
已知:①几种物质的溶解度(g/100gH2O)如表所示.

| FeSO4•7H2O | (NH4)2SO4 | FeSO4•(NH4)2SO4•6H2O | |
| 20℃ | 48 | 75 | 37 |
| 60℃ | 101 | 88 | 38 |
请回答:
(1)过滤所用的主要玻璃仪器为玻璃棒、漏斗、烧杯.
(2)溶液1中的主要溶质为FeSO4、H2SO4(填化学式).
(3)进行操作2时,从溶液中析出晶体后,需趁热过滤,原因为减小硫酸亚铁和硫酸铵的析出使得FeSO4•(NH4)2SO4•6H2O晶体更纯.
(4)FeSO4•(NH4)2SO4•6H2O用适量稀硫酸洗涤,而不是用水洗涤的原因为抑制亚铁离子和铵根离子的水解,防止亚铁离子被氧化.
(5)称取2.50gCuSO4•5H2O样品,灼烧过程中样品质量随温度(T)变化的曲线如图2所示.

①120℃所的固体,继续加热至258℃时失水,所发生反应的化学方程式为CuSO4•H2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+H2O.
②900℃时剩余固体只有一种铜的氧化物,其化学式为Cu2O.
8.下列实验能达到预期目的是( )
| 实验内容 | 实验目的 | |
| A | 向某未知溶液中加人BaCl2溶液后,再加人稀硝酸观察沉淀的生成 | 检验是否含 SO42-离子 |
| B | 向某未知溶液中加人NaOH固体,加热,在管口用湿润的蓝色石蕊试纸检验 | 检验是否含NH4+离子 |
| C | 加热分别用SO2和HClO漂白后的品红溶液 | 探究SO2和HCIO漂白原理的不同 |
| D | 加热盛有浓硫酸和铜的试管 | 探究浓硫酸的脱水性 |
| A. | A | B. | B | C. | C | D. | D |
5.运用化学反应原理研究物质的性质具有重要意义.请回答下列问题:
(1)请配平以下化学方程式:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
若反应过程中转移5mol电子,则生成标准状况下N2的体积为11.2L.
(2)25℃时,将a mol•L-1的氨水与0.1mol•L-1的盐酸等体积混合,当溶液中离子浓度关系满足c(NH4+)>c(Cl-)时,则反应的情况可能为a.
a.盐酸不足,氨水剩余b.氨水与盐酸恰好完全反应c.盐酸过量
(3)向NH4HSO4溶液中滴加少量的Ba(OH)2溶液的离子方程式2H++SO42-+Ba2++2OH-=BaSO4+2H2O.
(4)25℃,两种酸的电离平衡常数如表.
①HSO3-的电离平衡常数表达式K=$\frac{c(SO{\;}_{3}{\;}^{2-})c(H{\;}^{+})}{c(HSO{\;}_{3}{\;}^{-})}$.
②0.10mol•L-1Na2SO3溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
③H2SO3溶液和NaHCO3溶液混合,主要反应的离子方程式为H2SO3+HCO3-=HSO3-+CO2↑+H2O.
(1)请配平以下化学方程式:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
若反应过程中转移5mol电子,则生成标准状况下N2的体积为11.2L.
(2)25℃时,将a mol•L-1的氨水与0.1mol•L-1的盐酸等体积混合,当溶液中离子浓度关系满足c(NH4+)>c(Cl-)时,则反应的情况可能为a.
a.盐酸不足,氨水剩余b.氨水与盐酸恰好完全反应c.盐酸过量
(3)向NH4HSO4溶液中滴加少量的Ba(OH)2溶液的离子方程式2H++SO42-+Ba2++2OH-=BaSO4+2H2O.
(4)25℃,两种酸的电离平衡常数如表.
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
②0.10mol•L-1Na2SO3溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
③H2SO3溶液和NaHCO3溶液混合,主要反应的离子方程式为H2SO3+HCO3-=HSO3-+CO2↑+H2O.
2.体积为VmL,密度为ρg•mL-1的含有相对分子质量为M的某种物质(不含结晶水)的溶液,其中溶质为mg,其物质的量浓度为C mol/L,溶质的质量分数为W%,则下列表示正确的是( )
| A. | c=1000Wρ/M | B. | m=VρW/100 | C. | W%=cM/1000ρ% | D. | c=100m/VM |
3.用酸式滴定管准确移取25.00mL,某未知浓度的盐酸溶液于一洁净的锥形瓶中,然后用0.20mol•L-1的氢氧化钠溶液(指示剂为酚酞)滴定得结果如表
(1)根据以上数据可以计算出盐酸的物质的量浓度为0.16 mol•L-1.
(2)在配制250mL0.20mol•L-1的氢氧化钠标准溶液时,用到的仪器除托盘天平、烧杯、玻璃棒还有250mL容量瓶、胶头滴管.
(3)以下操作造成测定结果偏高的有DE.
A.配制标准溶液的氢氧化钠固体中混有KOH杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管.
| NaOH起始读数 | NaOH终点读数 | |
| 第一次 | 0.10ml | 20.30ml |
| 第二次 | 0.30ml | 20.10ml |
(2)在配制250mL0.20mol•L-1的氢氧化钠标准溶液时,用到的仪器除托盘天平、烧杯、玻璃棒还有250mL容量瓶、胶头滴管.
(3)以下操作造成测定结果偏高的有DE.
A.配制标准溶液的氢氧化钠固体中混有KOH杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管.
