题目内容
8.常温下,下列各组离子一定能在指定溶液中大量共存的是( )| A. | CuSO4溶液中:Na+、NH4+、K+、NO3-、Mg2+ | |
| B. | 使酚酞变红色的溶液中:NH4+、Zn2+、Cl-、NO3- | |
| C. | 水电离的c(H+)=1×10-13mol•L-1的溶液中:K+、Na+、AlO2-、SO32- | |
| D. | 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42- |
分析 A.五种离子之间不发生反应,都不与硫酸铜反应;
B.使酚酞变红色的溶液中存在大量氢氧根离子,铵根离子、锌离子与氢氧根离子反应;
C.水电离的c(H+)=1×10-13mol•L-1的溶液中存在大量氢离子或氢氧根离子,偏铝酸根离子、亚硫酸根离子与氢离子反应;
D.与Al反应能放出H2的溶液中存在大量氢离子或氢氧根离子,亚铁离子与氢氧根离子反应,酸性条件下硝酸根离子氧化亚铁离子.
解答 解:A.Na+、NH4+、K+、NO3-、Mg2+之间不反应,都不CuSO4与反应,在溶液中能够大量共存,故A正确;
B.使酚酞变红色的溶液为碱性溶液,溶液中存在大量氢氧根离子,NH4+、Zn2+与氢氧根离子反应,在溶液中不能大量共存,故B错误;
C.该溶液中存在大量氢离子或氢氧根离子,AlO2-、SO32-与氢离子反应,在溶液中不能大量共存,故C错误;
D.与Al反应能放出H2的溶液为酸性或强碱性溶液,Fe2+与与碱性溶液中的氢氧根离子反应,Fe2+、NO3-之间在酸性条件下发生氧化还原反应,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
18.下表是周期表中的一部分,根据①-⑩在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是Ne,只有负价而无正价的是F、O,还原性最强的单质是Na,可用于制半导体材料的元素是Si;
(2)最高价氧化物的水化物酸性最强的是HClO4,呈两性的是Al(OH)3,最高价氧化物的水化物碱性最强的是NaOH,电子式为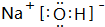 ;
;
(3)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是Na;
(4)比较⑥⑦⑨氢化物的稳定性最弱的是PH3;
(5)③元素单质和②元素最高价氧化物对应的水化物相互反应的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑;
(6)铍(Be)位于元素周期表中第二周期第ⅡA族.相同条件下,单质铍与酸反应比单质锂与酸反应更加缓慢(填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式Be+2HCl═BeCl2+H2↑.
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ④ | ⑦ | ⑧ | ⑩ | ||||
| 3 | ② | ③ | ⑤ | ⑥ | ⑨ |
(2)最高价氧化物的水化物酸性最强的是HClO4,呈两性的是Al(OH)3,最高价氧化物的水化物碱性最强的是NaOH,电子式为
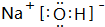 ;
;(3)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是Na;
(4)比较⑥⑦⑨氢化物的稳定性最弱的是PH3;
(5)③元素单质和②元素最高价氧化物对应的水化物相互反应的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑;
(6)铍(Be)位于元素周期表中第二周期第ⅡA族.相同条件下,单质铍与酸反应比单质锂与酸反应更加缓慢(填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式Be+2HCl═BeCl2+H2↑.
19.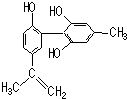 我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
 我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 滴入KMnO4(H+)溶液,观察紫色褪去,说明结构中有一定存在不饱和碳碳双键 | |
| C. | 1 mol该物质分别与浓溴水、H2反应时最多消耗Br2和H2分别为4mol、7 mol | |
| D. | 该分子中的所有原子有可能共平面 |
16.一个化学电池的总反应方程式为:Zn+Cu2+═Zn2++Cu,该化学电池的组成可能为( )
| A | B | C | D | |
| 正极 | Cu | Cu | Zn | Al |
| 负极 | Zn | Zn | Cu | Zn |
| 电解质溶液 | H2SO4 | CuSO4 | ZnCl2 | Cu Cl2 |
| A. | A | B. | B | C. | C | D. | D |
3.最近,科学家冶炼了纯度高达99.999%的铁,你估计它不会具有的性质是( )
| A. | 硬度比生铁低 | B. | 在潮湿空气中放置不易生锈 | ||
| C. | 可溶在稀H2S04中 | D. | 熔点比生铁低 |
13.如图所示:△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法正确的是( )
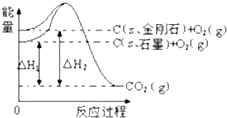

| A. | 石墨转化为金刚石需吸热 | B. | 石墨和金刚石的转化是物理变化 | ||
| C. | 金刚石的稳定性强于石墨 | D. | 石墨和金刚石是同分异构体 |
20.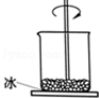 如图,小烧杯放在一块沾有水的玻璃片上,加入NH4Cl固体与氢氧化钡晶体[Ba(OH)2•8H2O],并用玻璃棒搅拌,玻璃片上的水结成了冰.由此可推断( )
如图,小烧杯放在一块沾有水的玻璃片上,加入NH4Cl固体与氢氧化钡晶体[Ba(OH)2•8H2O],并用玻璃棒搅拌,玻璃片上的水结成了冰.由此可推断( )
 如图,小烧杯放在一块沾有水的玻璃片上,加入NH4Cl固体与氢氧化钡晶体[Ba(OH)2•8H2O],并用玻璃棒搅拌,玻璃片上的水结成了冰.由此可推断( )
如图,小烧杯放在一块沾有水的玻璃片上,加入NH4Cl固体与氢氧化钡晶体[Ba(OH)2•8H2O],并用玻璃棒搅拌,玻璃片上的水结成了冰.由此可推断( )| A. | 该反应中,化学能转变成热能 | |
| B. | 反应物的总能量低于生成物的总能量 | |
| C. | 氯化铵与氢氧化钡的反应为放热反应 | |
| D. | 反应的热化学方程式为:2NH4Cl+Ba(OH)2═BaCl2+2NH3•H2O△H<0 |
8.化学与生活、社会发展息息相关,下列有关说法正确的是( )
| A. | 《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”,是用了KNO3的还原性 | |
| B. | 金属钠着火时,可直接用高压水枪喷水扑灭 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,这种提取青蒿素的过程属于化学变化 | |
| D. | 浓H2SO4具有腐蚀性,在其包装上应贴上 的危险警告标签 的危险警告标签 |
 在某有机物A的分子中,具有酚羟基、醇羟基、羧基等官能团,其结构简式如图.
在某有机物A的分子中,具有酚羟基、醇羟基、羧基等官能团,其结构简式如图.

 .
.