题目内容
能直接由金属单质与酸反应得到的盐是( )
| A、FeSO4 |
| B、CuCl2 |
| C、FeCl3 |
| D、AgCl |
考点:常见金属元素的单质及其化合物的综合应用
专题:元素及其化合物
分析:A.铁与稀硫酸反应生成硫酸亚铁;
B.金属活动性顺序表中,铜排在氢后面,铜不与盐酸反应;
C.铁与稀盐酸反应生成的是氯化亚铁,不会生成氯化铁;
D.金属活动性顺序表中,Ag排在氢后面,金属Ag不与盐酸反应.
B.金属活动性顺序表中,铜排在氢后面,铜不与盐酸反应;
C.铁与稀盐酸反应生成的是氯化亚铁,不会生成氯化铁;
D.金属活动性顺序表中,Ag排在氢后面,金属Ag不与盐酸反应.
解答:
解:A.铁可以直接与稀硫酸反应生成硫酸亚铁,能直接由金属单质与酸反应得到,故A正确;
B.由于铜活泼性较弱,金属铜不能直接与盐酸反应生成氯化铜,故B错误;
C.铁与稀盐酸直接反应生成氯化亚铁,只能用铁直接与盐酸反应生成氯化铁,故C错误;
D.金属银的活泼性较差,银单质不能与盐酸反应生成氯化银,故D错误;
故选A.
B.由于铜活泼性较弱,金属铜不能直接与盐酸反应生成氯化铜,故B错误;
C.铁与稀盐酸直接反应生成氯化亚铁,只能用铁直接与盐酸反应生成氯化铁,故C错误;
D.金属银的活泼性较差,银单质不能与盐酸反应生成氯化银,故D错误;
故选A.
点评:本题考查了金属与盐酸的反应产物判断,题目难度不大,试题侧重基础知识的考查,明确金属活动性顺序即可解答,注意铁与稀硫酸、盐酸的反应产物为氯化亚铁、硫酸亚铁,不是生成铁离子.

练习册系列答案
相关题目
下列物质的酸性强弱顺序为:H2A>H2B>HA->HB-,下列化学方程式中一定正确的是( )
| A、NaHB+H2A=H2B+NaHA |
| B、Na2B+H2A=H2B+Na2A |
| C、H2B+Na2A=Na2B+H2A |
| D、H2B+NaHA=NaHB+H2A |
1mol 下列物质与足量的银氨溶液作用,可还原出4mol Ag 的是( )
| A、丙醛 | B、乙二醛 | C、甲醛 | D、乙醛 |
把HI气体充入密闭容器中在一定条件下发生反应.2HI(g)?H2(g)+I2(g),在反应达到化学平衡,下列说法不正确的是( )
| A、HI的生成速率等于其分解速率 |
| B、各物质的浓度不变 |
| C、气体的颜色不变 |
| D、反应停止 |
有1体积的乙烯和乙炔的混合气体,恰好能跟相同条件下的1.6体积的H2完全反应生成乙烷,则混合气体中,乙烯和乙炔的物质的量之比是( )
| A、1:4 | B、3:7 |
| C、2:3 | D、2:1 |
如图是制取和收集某气体的实验装置,可用于( )
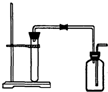

| A、用Zn粒与稀HCl反应制H2 |
| B、用Na2O2与H2O反应制O2 |
| C、用Cu与稀HNO3反应制NO |
| D、用MnO2与浓HCl反应制Cl2 |
实验室中保存下列化学药品的方法不妥当的是( )
| A、将AgNO3晶体放在棕色试剂瓶中 |
| B、NaOH溶液保存在带橡胶塞的细口试剂瓶中 |
| C、金属钾、钠和非金属白磷保存在煤油中 |
| D、浓硝酸溶液保存在棕色试剂瓶中 |
室温下,pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是( )
| A、使温度都升高20℃后,两溶液的pH均不变 |
| B、加相同量的水稀释,两溶液的pH变化程度相同 |
| C、加足量的锌时,刚开始反应醋酸产生的氢气比盐酸快 |
| D、加足量的锌充分反应后,醋酸产生的氢气比盐酸多 |
 某课外活动小组设计了如图所示的装置,自制氢氧燃料电池.图中电解质溶液为0.5mol/LNa2SO4(aq),电源用3~6V直流电源,发光二极管起辉电压1.7V,电流为0.6mA.
某课外活动小组设计了如图所示的装置,自制氢氧燃料电池.图中电解质溶液为0.5mol/LNa2SO4(aq),电源用3~6V直流电源,发光二极管起辉电压1.7V,电流为0.6mA.