题目内容
为增大氯水中c(HClO),应采取的措施是( )
| A、加入KOH固体 |
| B、加入氯化钾固体 |
| C、加入CaCO3 |
| D、加入Na2SO3固体 |
考点:化学平衡的影响因素
专题:
分析:溶液中存在平衡:Cl2+H2O?H++Cl-+HClO,增大氯水中的HClO浓度,应改变条件是平衡向正反应方向移动,但不能加水稀释、不能加入与HClO反应的物质,据此结合平衡移动原理解答.
解答:
解:A.加入KOH固体,KOH与HClO反应生成次氯酸钾,溶液中HClO浓度减小,故A不符合;
B.加入氯化钾固体,溶液中氯离子浓度增大,平衡向左移动,溶液中HClO浓度减小,故B不符合;
C.加入CaCO3固体,与氢离子反应,导致溶液中氢离子浓度降低,平衡向右移动,溶液中HClO浓度增大,故C符合;
D.亚硫酸钠具有还原性,加入亚硫酸钠固体,与氯气反应,溶液中氯气浓度减小、氢离子浓度增大,平衡向左移动,溶液中HClO浓度减小,故D不符合;
故选C.
B.加入氯化钾固体,溶液中氯离子浓度增大,平衡向左移动,溶液中HClO浓度减小,故B不符合;
C.加入CaCO3固体,与氢离子反应,导致溶液中氢离子浓度降低,平衡向右移动,溶液中HClO浓度增大,故C符合;
D.亚硫酸钠具有还原性,加入亚硫酸钠固体,与氯气反应,溶液中氯气浓度减小、氢离子浓度增大,平衡向左移动,溶液中HClO浓度减小,故D不符合;
故选C.
点评:本题考查影响化学平衡的因素,难度不大,注意D选项中氯气反应的影响是主要因素.

练习册系列答案
相关题目
类推是化学学习中常用的方法,但在具体应用的时候,还应注意反常的一些现象,下列类推正确的一项( )
| A、CH4的熔沸点低于SiH4,类推NH3的沸点低于PH3 |
| B、二氧化碳是分子晶体,类推二氧化硅也是分子晶体 |
| C、CaCO3的溶解度低于Ca(HCO3)2,类推Na2CO3溶解度低于NaHCO3 |
| D、H2O的空间构型是“V”形,类推H2S也是“V”形 |
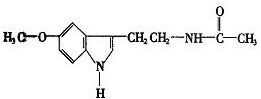 脑白金的主要作用是改善睡眠和润肠通便,主要成分是褪黑素(Melatonin)和低聚糖,其有效成分的结构简式如图,下列对该化合物的叙述正确的是( )
脑白金的主要作用是改善睡眠和润肠通便,主要成分是褪黑素(Melatonin)和低聚糖,其有效成分的结构简式如图,下列对该化合物的叙述正确的是( )①它属于芳香烃
②分子式为C15N2H16O2
③可以使酸性高锰酸钾溶液褪色
④不可以发生水解反应.
| A、②③ | B、③ | C、③④ | D、①②④ |
欲除去氢氧化钠溶液中混有的少量碳酸钠,下列方法中最适当的是( )
| A、加入适量的稀硫酸 |
| B、加入适量的盐酸 |
| C、加入适量的氢氧化钙溶液 |
| D、加入适量的氯化钙溶液 |