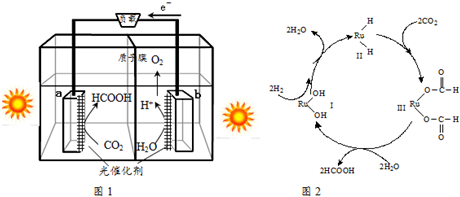
��Ŀ����
12������������Ԫ��X��Y��Z��W��Rԭ��������������Xԭ�ӵ������������Ǵ�����3����Y��X���γ����ӻ�����Y2X��Y2X2��Z���ڵ�������������������λ�ã�W�ĵ��ʹ㷺�����뵼����ϣ�R�ij������ϼ�Ϊ-1��+1��+4��+5��+7��������������ȷ���ǣ�������| A�� | WX2���������ά��ԭ�� | |
| B�� | RX2����������ˮ�������� | |
| C�� | ��ҵ�ϻ�õ���Y���������Ȼ�ԭYR�õ� | |
| D�� | Y��Z��R������������ˮ��������֮����ܷ�����Ӧ |
���� ����������Ԫ��X��Y��Z��W��Rԭ��������������Xԭ�ӵ������������Ǵ�����3������X����2�����Ӳ㣬����㺬��6�����ӣ�ΪOԪ�أ�Y��X���γ����ӻ�����Y2X��Y2X2����X+1�ۣ�ΪNaԪ�أ�Z���ڵ�������������������λ�ã�Zλ�ڵ������ڣ���ZΪAlԪ�أ�W�ĵ��ʹ㷺�����뵼����ϣ���WΪSiԪ�أ�R�ij������ϼ�Ϊ-1��+1��+4��+5��+7��R�����Ϊ+7����ԭ����������Si����RΪClԪ�أ��ݴ˽��Ԫ��������֪ʶ���
��� �⣺����������Ԫ��X��Y��Z��W��Rԭ��������������Xԭ�ӵ������������Ǵ�����3������X����2�����Ӳ㣬����㺬��6�����ӣ�ΪOԪ�أ�Y��X���γ����ӻ�����Y2X��Y2X2����X+1�ۣ�ΪNaԪ�أ�Z���ڵ�������������������λ�ã�Zλ�ڵ������ڣ���ZΪAlԪ�أ�W�ĵ��ʹ㷺�����뵼����ϣ���WΪSiԪ�أ�R�ij������ϼ�Ϊ-1��+1��+4��+5��+7��R�����Ϊ+7����ԭ����������Si����RΪClԪ�أ�
A��WX2��SiO2�������������������ά��ԭ�ϣ���A��ȷ��
B��RX2ΪClO2��ClO2����ǿ�����ԣ�����������ˮ������������B��ȷ��
C��YΪNaԪ�أ���ҵ�ϻ�õ���Na��ͨ���������NaCl��ã�����������ԭ����C����
D��Y��Z��R������������ˮ����ֱ�ΪNaOH���������������ᣬ����֮���������ܷ�����Ӧ����D��ȷ��
��ѡC��
���� ���⿼����ԭ�ӽṹ��Ԫ�������ɵĹ�ϵ����Ŀ�Ѷ��еȣ��ƶ�Ԫ��Ϊ���ؼ���ע����������Ԫ�����ڱ��ṹ��Ԫ�����������ݣ��������������ѧ���ķ���������������������

| A�� | ��״�ٻ��ܿ��� | B�� | ���Ͳ� | C�� | �ط��Լ�״���� | D�� | ���Լ��ؼ��� |
�ף���500��ʱ��10mol SO2��5mol O2��Ӧ
�ң���500��ʱ����V2O5��������10mol SO2��5mol O2��Ӧ
������450��ʱ��8mol SO2��5mol O2��Ӧ
������500��ʱ��8mol SO2��5mol O2��Ӧ��
| A�� | �ס��ҡ������� | B�� | �ҡ��ס������� | C�� | �ҡ��ס������� | D�� | ���������ҡ��� |
| A�� | �õ�ˮ���������Һ��������Һ | |
| B�� | �����Ը��������Һ������ϩ����Ȳ | |
| C�� | ����ˮ�������Ȼ�̼�ͱ�������ɫҺ�� | |
| D�� | �ý����Ƽ����Ҵ�������ѣ�CH3OCH3�� |
��п����пƬ
���
��10%������
��20%������
��98%������
����
���ñ���ȴ
��Ͻ���
��Ѹ�ټ���п���ã�
| A�� | �ڢݢߢ� | B�� | �٢ܢ�� | C�� | �ۢݢߢ� | D�� | �ۢޢߢ� |
�ټ�KNO3���塡
�ڼ�NaOH���塡
�۵��뼸��Ũ���ᡡ
�ܼ�CH3COONa���塡
�ݼ�NaCl��Һ��
���뼸������ͭ��Һ��
�������¶ȡ�
�����10mL 1mol/L���ᣮ
| A�� | �٢ޢ� | B�� | �ۢݢ� | C�� | �ޢߢ� | D�� | �ۢߢ� |
| A�� | ��ϩ���Ҵ����������ơ�CaCl2�����зǼ��Լ� | |
| B�� | �Ҵ������ᡢˮ�����о�������� | |
| C�� | �ױ������й�ƽ���ԭ�������13�� | |
| D�� | BF3��PCl3��CCl4����������ԭ��ȫ�����������Ϊ8�����ӽṹ |