题目内容
将 0.195g锌粉加入到20.0mL的0.100 mol·L-1MO2+溶液中,恰好完全反应,则还原产物可能是
A.M B.M2+ C.M3+ D.MO2+
B
【解析】
试题分析:根据氧化还原反应中氧化剂和还原剂之间得失电子数目相等计算反应后M元素的化合价,n(Zn)=0.195/65=0.003mol,n(MO2+)=0.02L×0.100mol?L-1=0.002mol,
设反应后M的化合价为+x价,则(5-x)×0.002mol=0.003mol×(2-0),x=2,选B.
考点:考查氧化还原反应。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列关于离子共存的评价及离子方程式书写正确的是
选项 | 离子组 | 评价 |
A | H+、Mg2+、Br-、NO3- | 能大量共存于同一溶液中,投入少量锌粉后,可放出H2 ,反应的离子方程式为 Zn+ 2H+ = Zn2++ H2↑ |
B | NH4+、CO32-、Cl-、Al3+ | 不能大量共存于同一溶液中,因为有沉淀生成 2Al3++3CO32-=Al2(CO3)3↓ |
C | ClO-、Na+、K+、HSO3- | 能大量共存于同一溶液中 |
D | HCO3-、OH-、Na+、K+ | 不能大量共存于同一溶液中,因为发生如下反应 HCO3-+ OH-= CO32-+ H2O |
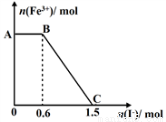
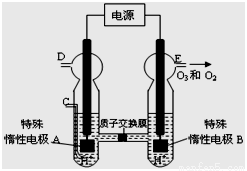
 NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是
NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是