题目内容
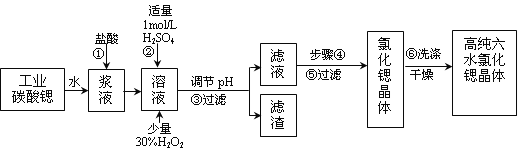
【题目】工业上用难溶于水的碳酸锶(SrCO3)粉末为原料(含少量钡和铁的化合物)制备高纯六水氯化锶晶体(SrCl2·6H2O),其过程为:
已知:Ⅰ.有关氢氧化物沉淀的pH:
氢氧化物 | Fe(OH)3 | Fe(OH)2 |
开始沉淀的pH | 1.5 | 6.5 |
沉淀完全的pH | 3.7 | 9.7 |
Ⅱ.SrCl2·6H2O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
(1)操作①需要加快反应速率,措施有充分搅拌和____________________(写一种)。碳酸锶与盐酸反应的离子方程式________________________________。
(2)在步骤②~③的过程中,将溶液的pH值由1调节至_______;宜用的试剂为_______。
A.1.5 B.3.7 C.9.7 D.氨水 E.氢氧化锶粉末 F.碳酸钠晶体
(3)操作③中所得滤渣的主要成分是_______________________(填化学式)。
(4)工业上用热风吹干六水氯化锶,适宜的温度是_______。
A.50~60℃ B.80~100℃ C.100℃以上
(5)步骤⑥宜选用的无机洗涤剂是_______________。
【答案】加热、适当增加盐酸浓度 SrCO3+2H+=Sr2++CO2↑+H2O B E Fe(OH)3、BaSO4 A 饱和氯化锶溶液
【解析】
以SrCO3为原料制备六水氯化锶(SrCl26H2O),由流程可知,SrCO3和盐酸发生反应:SrCO3+2HCl=SrCl2+CO2↑+H2O,反应后溶液中除含有Sr2+和Cl-外,还含有少量Fe2+、Ba2+杂质,加入过氧化氢,将Fe2+氧化为Fe3+,然后加硫酸生成硫酸钡沉淀,同时调节溶液pH,使Fe3+转化氢氧化铁沉淀,所以过滤后滤渣为硫酸钡和氢氧化铁,滤液中含SrCl2,最后蒸发、冷却结晶得到SrCl26H2O。据此解答。
(1)加快反应速率,可通过增大反应物浓度、加热、搅拌、增大接触面积等,碳酸锶与盐酸反应生成氯化锶、二氧化碳和水,反应的离子方程式为SrCO3+2H+=Sr2++CO2↑+H2O;
(2)在步骤②~③的过程中,Fe2+被H2O2氧化为Fe3+,调节pH就是为了除去Fe3+,Fe3+完全沉淀的pH是3.7,所以应将溶液的pH值由1调节至3.7,但不能引入杂质,最好选用氢氧化锶粉末;答案选BE;
(3)碳酸锶中含少量钡的化合物,加入了稀硫酸,所以有硫酸钡生成,调节pH可生成氢氧化铁沉淀,所以操作③中所得滤渣的主要成分是Fe(OH)3、BaSO4;
(4)SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水,所以用热风吹干六水氯化锶的温度不能高于61℃,答案选A;
(5)步骤⑥得到SrCl2·6H2O,所以选用的无机洗涤剂是饱和氯化锶溶液,既不引入杂质,也能减小晶体的溶解。

 全能测控一本好卷系列答案
全能测控一本好卷系列答案【题目】现有常温下的四种溶液(如下表),下列有关叙述中正确的是( )
① | ② | ③ | ④ | |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 硫酸 |
pH | 11 | 11 | 3 | 3 |
A.在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变
B.V1L④与V2L②溶液混合后,若混合后溶液pH=4,则V1:V2=9:11
C.分别加水稀释10倍、四种溶液的pH:①>②>③>④
D.将①、④两种溶液等体积混合,所得溶液中:c(NH4+)>c(SO42-)>c(OH-)>c(H+)
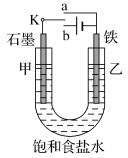
【题目】根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
① 连接仪器、________、加药品后,打开a关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是_______。装置A中试剂是_______。
③ 能说明碳的非金属性比硅强的实验现象是_________。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是____。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
滴加的溶液 | 氯水 | 氨水 |
沉淀的化学式 | ____ | ____ |
写出其中SO2显示还原性生成沉淀的离子方程式_________。
【题目】80℃时,1L 密闭容器中充入0.20 mol N2O4,发生反应N2O4![]() 2NO2 △H = + Q kJ·mol﹣1(Q>0),获得如下数据:
2NO2 △H = + Q kJ·mol﹣1(Q>0),获得如下数据:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol·L﹣1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
下列判断正确的是
A. 升高温度该反应的平衡常数K减小
B. 20~40s 内,v(N2O4)= 0.004 mol·L-1·s-1
C. 100s时再通入0.40 mol N2O4,达新平衡时N2O4的转化率增大
D. 反应达平衡时,吸收的热量为0.15Q kJ