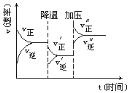
题目内容
【题目】根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
① 连接仪器、________、加药品后,打开a关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是_______。装置A中试剂是_______。
③ 能说明碳的非金属性比硅强的实验现象是_________。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是____。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
滴加的溶液 | 氯水 | 氨水 |
沉淀的化学式 | ____ | ____ |
写出其中SO2显示还原性生成沉淀的离子方程式_________。
【答案】检验装置气密性 Cu + 2H2SO4(浓)![]() CuSO4 + SO2↑+ 2H2O KMnO4溶液 A中KMnO4溶液没有完全褪色,盛有Na2SiO3溶液的试管中出现白色沉淀 2H2S+SO2=3S↓+2H2O BaSO4 BaSO3 Ba2++SO2+Cl2+2H2O═BaSO4↓+4H++2Cl-
CuSO4 + SO2↑+ 2H2O KMnO4溶液 A中KMnO4溶液没有完全褪色,盛有Na2SiO3溶液的试管中出现白色沉淀 2H2S+SO2=3S↓+2H2O BaSO4 BaSO3 Ba2++SO2+Cl2+2H2O═BaSO4↓+4H++2Cl-
【解析】
(1)①验证碳、硅非金属性的相对强弱,是通过碳酸和可溶性硅酸盐反应析出硅酸沉淀实现的,所以为了保证实验效果和实验的顺利进行,须检查装置的气密性;
②铜与浓硫酸反应,铜被氧化成+2价的铜离子,硫酸被还原成+4价的二氧化硫;高锰酸钾有强氧化性,能氧化二氧化硫;
③当A中KMnO4溶液没有完全褪色,说明二氧化硫已经完全除尽,盛有Na2SiO3溶液的试管中出现白色沉淀,说明碳的非金属性比硅强;
(2)②二氧化硫中硫元素的化合价是+4价,被硫化氢中-2价的硫还原;
③氯气具有氧化性,能将二氧化硫氧化成+6价的硫酸根离子,硫酸根离子和钡离子反应生成硫酸钡沉淀。
(1)①为了保证实验的顺利进行,避免装入药品后发现装置气密性不好,更换部分仪器而浪费药品,避免装置漏气影响实验效果,所以连接仪器后须检查装置气密性;
②铜和热的浓硫酸反应,反应中Cu元素的化合价由0升高到+2价,作还原剂,产物为二氧化硫、硫酸铜和水,反应的方程式为Cu + 2H2SO4(浓)![]() CuSO4 + SO2↑+ 2H2O ;高锰酸钾有氧化性,二氧化硫和高锰酸钾能发生氧化还原反应;
CuSO4 + SO2↑+ 2H2O ;高锰酸钾有氧化性,二氧化硫和高锰酸钾能发生氧化还原反应;
③二氧化硫中硫元素的化合价是+4价,属于中间价态,既有氧化性又有还原性,高锰酸钾有强氧化性,离子方程式为5SO2+2MnO4-+2H2O═2Mn2++5SO42-+4H+,当A中KMnO4溶液没有完全褪色,说明二氧化硫已经完全除尽,避免了二氧化硫和可溶性硅酸盐反应,二氧化碳和水反应生成碳酸,碳酸和可溶性硅酸盐反应析出硅酸白色沉淀,说明碳酸能制取硅酸,能证明碳酸酸性强于硅酸酸性;
(2)②二氧化硫中硫元素的化合价是+4价,有氧化性,二氧化硫气体与H2S溶液常温下反应,生成黄色固体硫(单质)和水,反应的化学方程式为2H2S + SO2 = 3S↓ + 2H2O;
③BaCl2溶液中无明显现象,将其分成两份,一份滴加氯水溶液,氯水中有氯气分子,氯气分子具有氧化性,能把二氧化硫氧化成+6价的硫酸根离子,硫酸根离子和钡离子反应生成BaSO4白色沉淀,反应的方程式为Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-,另一份中滴加氨水,二氧化硫和水生成亚硫酸,亚硫酸和氨水反应生成亚硫酸铵,亚硫酸铵电离出氨根离子和亚硫酸根离子,亚硫酸根离子和钡离子反应生成BaSO3沉淀。

【题目】工业上用难溶于水的碳酸锶(SrCO3)粉末为原料(含少量钡和铁的化合物)制备高纯六水氯化锶晶体(SrCl2·6H2O),其过程为:
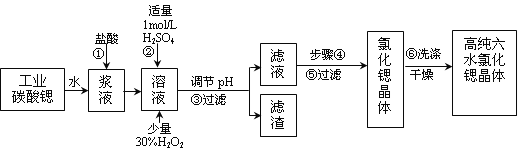
已知:Ⅰ.有关氢氧化物沉淀的pH:
氢氧化物 | Fe(OH)3 | Fe(OH)2 |
开始沉淀的pH | 1.5 | 6.5 |
沉淀完全的pH | 3.7 | 9.7 |
Ⅱ.SrCl2·6H2O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
(1)操作①需要加快反应速率,措施有充分搅拌和____________________(写一种)。碳酸锶与盐酸反应的离子方程式________________________________。
(2)在步骤②~③的过程中,将溶液的pH值由1调节至_______;宜用的试剂为_______。
A.1.5 B.3.7 C.9.7 D.氨水 E.氢氧化锶粉末 F.碳酸钠晶体
(3)操作③中所得滤渣的主要成分是_______________________(填化学式)。
(4)工业上用热风吹干六水氯化锶,适宜的温度是_______。
A.50~60℃ B.80~100℃ C.100℃以上
(5)步骤⑥宜选用的无机洗涤剂是_______________。